
【题目】25℃时,用Na2S沉淀Cu2+、Zn2+两种金属阳离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如图所示。下列说法不正确的是( )

A.向Cu2+浓度为1×10-5mol·L-1的工业废水中加入ZnS粉末,会有CuS沉淀析出
B.25℃时,Ksp(CuS)约为1×10-35
C.向100mLZn2+、Cu2+浓度均为1×10-5 mol·L-1的混合溶液中逐滴加入1×10-4mol·L-1的Na2S溶液,Cu2+先沉淀
D.Na2S溶液中:c(H+)+c(HS-)+c(H2S)=c(OH-)
【答案】D
【解析】
B.正确,因25℃时,当横坐标lgc(S2-)= -10时,纵坐标lgc(M2+)= -25(图中原点位),故Ksp(CuS)约为1×10-35;
C.正确,向100 mL Zn2+、Cu2+浓度均为10-5 mol/L的混合溶液中逐滴加入10-4 mol/L的Na2S溶液,Cu2+先沉淀,因为Ksp(CuS)<Ksp(ZnS);
A.向Cu2+浓度为10-5 mol/L的工业废水中加入ZnS粉末,会有CuS沉淀析出,因为Ksp(CuS)<Ksp(ZnS),故ZnS可以转化为更难溶的CuS。故A选项正确。
B.因25℃时,当横坐标lgc(S2-)= -10时,纵坐标lgc(M2+)= -25(图中原点位),故Ksp(CuS)约为1×10-35,故B选项正确。
C.向100 mL Zn2+、Cu2+浓度均为10-5 mol/L的混合溶液中逐滴加入10-4 mol/L的Na2S溶液,Cu2+先沉淀,因为Ksp(CuS)<Ksp(ZnS),故B选项正确。
D.由物料守恒可知应为2c(S2-)+2c(HS-)+2c(H2S)=c(Na+),故c(H+)+c(HS-)+2c(H2S)=c(OH-),故D选项错误。
故答案选D。


科目:高中化学 来源: 题型:
【题目】室温下,用![]() 的
的![]() 溶液滴定
溶液滴定![]()
![]() 的
的![]() 溶液,水的电离程度随
溶液,水的电离程度随![]() 溶液体积的变化曲线如图所示。下列说法正确的是( )
溶液体积的变化曲线如图所示。下列说法正确的是( )

A.该滴定过程应该选择甲基橙作为指示剂
B.从![]() 点到
点到![]() 点,溶液中水的电离程度逐渐增大
点,溶液中水的电离程度逐渐增大
C.![]() 点溶液中
点溶液中![]()
D.![]() 点对应的
点对应的![]() 溶液的体积为
溶液的体积为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物A(C8H8O2)为一种无色液体。从A出发可发生如图的一系列反应。则下列说法正确的是

A.A的结构中含有碳碳双键
B.G的同分异构体中属于酯且能发生银镜反应的只有一种
C.上述各物质中能发生水解反应的有A、B、D、G
D.根据图示可推知D为苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,aL密闭容器中加入1molN2和3molH2发生N2+3H2![]() 2NH3的反应,下列叙述中能说明该反应已达到化学平衡状态的是( )
2NH3的反应,下列叙述中能说明该反应已达到化学平衡状态的是( )
A.v(N2正)=2v(NH3正)
B.3v(H2正)=v(N2逆)
C.单位时间内有0.3molH2消耗的同时,生成0.2molNH3
D.单位时间内有1个N≡N键断裂的同时,有6个N—H键断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是( )
A.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中![]() 不变
不变
B.将CH3COONa溶液从20℃升温至30℃,溶液中![]() 增大
增大
C.向盐酸中加入氨水至中性,溶液中![]() >1
>1
D.向0.1molL-1CH3COOH 溶液中加入少量水,溶液中 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】G是一种治疗急慢性呼吸道感染的特效药中间体,其制备路线如图:

(1)化合物C中的含氧官能团是_____。
(2)A→B的反应类型是______。
(3)化合物F的分子式为C14H21NO3,写出F的结构简式______。
(4)从整个制备路线可知,反应B→C的目的是______。
(5)同时满足下列条件的B的同分异构体共有_______种。
①分子中含有苯环,能与NaHCO3溶液反应;
②能使FeCl3溶液显紫色
(6)根据已有知识并结合相关信息,完成以![]() 、CH3NO2为原料制备
、CH3NO2为原料制备 的合成路线图____(无机试剂任用,合成路线流程图示例见本题题干)。
的合成路线图____(无机试剂任用,合成路线流程图示例见本题题干)。
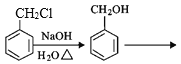
 ,其中第二步反应的方程式为_____。
,其中第二步反应的方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳的回收利用是环保领域研究的热点课题。
(1)以CO2与NH3为原料合成尿素[CO(NH2)2]的技术已十分成熟。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) △H=-159.47 kJmol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(l) △H=+28.49kJmol-1
③H2O(g)=H2O(l) △H=-88.0kJmol-1
则NH3和CO2合成尿素和气态水的热化学方程式为___。
(2)已知:工业上在120℃条件下利用NH3和CO2合成尿素。在恒温恒容条件下,下列能说明合成尿素反应达平衡的是___
A.NH3和CO2的比例保持不变
B.混合气体的压强不再发生变化
C.2v(NH3)(正)=v(CO2)(逆)
D.混合气体的密度不再改变
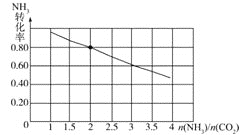
(3)氨碳比[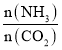 ]对合成尿素有重要影响。恒温恒容条件下,在一个2L的密闭容器中将总物质的量为nmol的NH3和CO2以不同的氨碳比进行反应,NH3的转化率变化如图所示;当[
]对合成尿素有重要影响。恒温恒容条件下,在一个2L的密闭容器中将总物质的量为nmol的NH3和CO2以不同的氨碳比进行反应,NH3的转化率变化如图所示;当[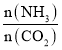 ]=2时,平衡吋测得尿素的物质的量为1mol,则n=___。此温度下该反应的化学平衡常数K=___。
]=2时,平衡吋测得尿素的物质的量为1mol,则n=___。此温度下该反应的化学平衡常数K=___。
(4)研究人员设计出一种新型太阳能电池,能直接把CO2和H2O转化为CO、H2和O2,原理如图所示,该装置中能量转化方式为___,催化剂b表面的电极反应式为___。
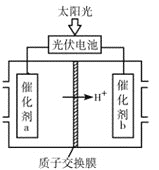
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组在实验室用乙醇、浓硫酸和溴化钠和水混合反应来制备溴乙烷,并探究溴乙烷的性质。
有关数据见下表:
乙醇 | 溴乙烷 | 溴 | |
状态 | 无色液体 | 无色液体 | 深红色液体 |
密度/(g·cm3) | 0.79 | 1.44 | 3.1 |
沸点/℃ | 78.5 | 38.4 | 59 |
一.溴乙烷的制备
反应原理和实验装置如下(加热装置、夹持装置均省略):
H2SO4+NaBr![]() NaHSO4+HBr↑ CH3CH2OH+HBr
NaHSO4+HBr↑ CH3CH2OH+HBr![]() CH3CH2Br+H2O
CH3CH2Br+H2O
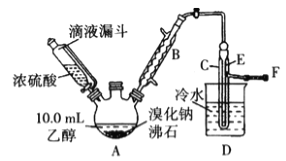
(1)图中沸石的作用为_____________。若图甲中A加热温度过高或浓硫酸的浓度过大,均会使C中收集到的粗产品呈橙色,原因是A中发生了副反应生成了________;F连接导管通入稀NaOH溶液中,其目的主要是吸收_________等防止污染空气;导管E的末端须低于D中烧杯内的水面,其目的是_______________________________。
(2)粗产品用上述溶液洗涤、分液后,再经过蒸馏水洗涤、分液,然后加入少量的无水硫酸镁固体,静置片刻后过滤,再将所得滤液进行蒸馏,收集到的馏分约10.0g。从乙醇的角度考虑,本实验所得溴乙烷的产率是_____________(保留3位有效数字)。
二.溴乙烷性质的探究
用如图实验装置验证溴乙烷的性质:
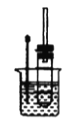
(3)在乙中试管内加入10mL6mol·L-1NaOH溶液和2mL溴乙烷,振荡、静置,液体分层,水浴加热。该过程中的化学方程式为_______________________________________,证明溴乙烷与NaOH溶液已反应完全的现象是________________________________。
(4)若将乙中试管里的NaOH溶液换成NaOH乙醇溶液,为证明产物为乙烯,将生成的气体通入如图装置。a试管中的水的作用是________________;若无a试管,将生成的气体直接通入b试管中,则b中的试剂可以为______________。
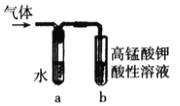
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com