
| A�� | ԭ�Ӱ뾶��W��Z��Y��X��M | |
| B�� | ��XZ2ͨ��W������ˮ��Ӧ�����Һ�У����ɵ���һ��ֻ��һ�� | |
| C�� | ��X��Y��Z��M����Ԫ�ع�ͬ�γɵĻ�������һ���й��ۼ����������Ӽ� | |
| D�� | CaX2��CaM2����CaZ2��3�ֻ������У��������������Ӹ����Ⱦ�Ϊ1��2 |
���� X��Y��Z����Ԫ����ԭ���������ε�����ͬ����Ԫ�أ�������������֮��Ϊ15������������ƽ��Ϊ5��X��Z���γ�XZ2��̬���ӣ�XΪ+4�ۣ�YΪ-2�ۣ����Ƴ�X��Y��Z�ֱ�ΪC��N��O����Ԫ�أ�
����Y��M�γɵ���̬�������ڱ�״���µ��ܶ�0.76g•L-1���Ϳɼ��������̬�������Ħ������Ϊ22.4L/mol��0.76g•L-1=17g/mol���Ӷ�ȷ��MΪHԪ�أ�
����W����������X��Y��Z��M����Ԫ��������֮�͵�$\frac{1}{2}$���Ƴ�W��������Ϊ$\frac{1}{2}$��6+7+8+1��=11������WΪNaԪ�أ���϶�Ӧ���ʡ�������������Լ�Ԫ��������֪ʶ�����⣮
��� �⣺X��Y��Z����Ԫ����ԭ���������ε�����ͬ����Ԫ�أ�������������֮��Ϊ15������������ƽ��Ϊ5��X��Z���γ�XZ2��̬���ӣ�XΪ+4�ۣ�YΪ-2�ۣ����Ƴ�X��Y��Z�ֱ�ΪC��N��O����Ԫ�أ�
����Y��M�γɵ���̬�������ڱ�״���µ��ܶ�0.76g•L-1���Ϳɼ��������̬�������Ħ������Ϊ22.4L/mol��0.76g•L-1=17g/mol���Ӷ�ȷ��MΪHԪ�أ�
����W����������X��Y��Z��M����Ԫ��������֮�͵�$\frac{1}{2}$���Ƴ�W��������Ϊ$\frac{1}{2}$��6+7+8+1��=11������WΪNaԪ�أ�
A��ͬ������������ԭ�Ӱ뾶��С��ͬ�������ϵ���ԭ�Ӱ뾶����ԭ�Ӱ뾶Na��C��N��O��H����W��X��Y��Z��M���ʴ���
B��W���ʵ�ˮ��ҺΪNaOH��Һ����CO2ͨNaOH����Һ�У����ɵ��ο���Ϊ̼���ơ�̼�����ƻ���߶��У���B����
C��X��Y��Z��M��Ϊ�ǽ���Ԫ�أ�����Ԫ���γɵĻ�����һ�����й��ۼ������ܺ������Ӽ�����̼��李�����淋����ʣ���C��ȷ��
D��CaC2��CaO2�У��������������Ӹ�����Ϊ1��1��CaH2�������ӡ������Ӹ���֮��Ϊ1��2����D����
��ѡC��
���� ���⿼��Ԫ���ƶϡ�Ԫ�������ɡ����ӽṹ��C��N��NaԪ�ػ��������ʵȣ�Ϊ�߿��������ͣ�������ѧ���ķ��������Ŀ��飬�Ѷ��еȣ������ܶ��ж�Y��M�γɵ���̬�������ǰ���Ϊ�ƶϵĹؼ���ע��X��ZԪ���ƶ���ż�Ե����ã�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
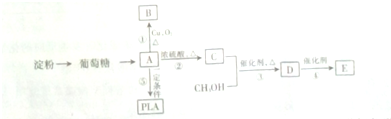
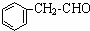 ����Ҫ��������Ҷ�У���Ũ�������������������ںϳ����ϣ���������ת����ϵ������C��ʹ������Ȼ�̼��Һ��ɫ��E��������������F��F����Է�������Ϊ90��
����Ҫ��������Ҷ�У���Ũ�������������������ںϳ����ϣ���������ת����ϵ������C��ʹ������Ȼ�̼��Һ��ɫ��E��������������F��F����Է�������Ϊ90��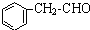 $\stackrel{HCN}{��}$A$��_{H_{2}O}^{HCl}$B$��_{��}^{ŨH_{2}SO_{4}}$C$��_{��Zn/H_{2}O}^{��O_{3}}$D+E
$\stackrel{HCN}{��}$A$��_{H_{2}O}^{HCl}$B$��_{��}^{ŨH_{2}SO_{4}}$C$��_{��Zn/H_{2}O}^{��O_{3}}$D+E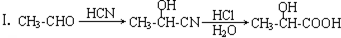
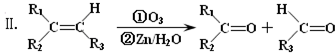
 ���÷�Ӧ��������ȥ��Ӧ��
���÷�Ӧ��������ȥ��Ӧ��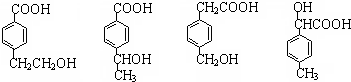 ����һ�֣�
����һ�֣��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
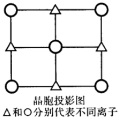 X��Y��Z��W��Q����ǰ������Ԫ�أ�ԭ����������������֪X��Y��Z��W��Ϊ�ǽ���Ԫ�أ�XW2������Y3-Ϊ�ȵ����壬Ԫ��W��ԭ����������Ԫ��Z��ԭ��������8��Q������������Ϊ2����������������Y��W2-����������֮�ͣ�����������Ϣ�ش��������⣺
X��Y��Z��W��Q����ǰ������Ԫ�أ�ԭ����������������֪X��Y��Z��W��Ϊ�ǽ���Ԫ�أ�XW2������Y3-Ϊ�ȵ����壬Ԫ��W��ԭ����������Ԫ��Z��ԭ��������8��Q������������Ϊ2����������������Y��W2-����������֮�ͣ�����������Ϣ�ش��������⣺ ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
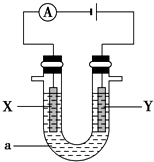
 �ס������������У��ֱ����0.1 mol•L -1�� NaCl��Һ��0.1 mol•L-1��AgNO3��Һ���� PtΪ�缫���е��ʱ����A��B��C��D���缫������������ʵ���֮��Ϊ ��������
�ס������������У��ֱ����0.1 mol•L -1�� NaCl��Һ��0.1 mol•L-1��AgNO3��Һ���� PtΪ�缫���е��ʱ����A��B��C��D���缫������������ʵ���֮��Ϊ ��������| A�� | 2��2��4��1 | B�� | 2��3��4��1 | C�� | 1��4��2��2 | D�� | 1��1��1��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
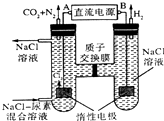
| A�� | BΪ��Դ������ | |
| B�� | ����������������Һ��pH����ǰ��Ƚ����� | |
| C�� | �����ƶ��ķ�����B���Ҳ���Ե缫�������Ե缫��A | |
| D�� | �������з����ķ�Ӧ����Ϊ2Cl--2e-=Cl2����CO��NH2��2+3Cl2+H2O�TN2+CO2+6HCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
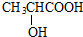 C�����������ŵ��������Ȼ���̼̼˫��
C�����������ŵ��������Ȼ���̼̼˫��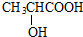 +O2$��_{��}^{Cu}$
+O2$��_{��}^{Cu}$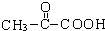 +2H2O��Ӧ�ܵĻ�ѧ����ʽΪn CH2=CHCOOCH3$\stackrel{����}{��}$
+2H2O��Ӧ�ܵĻ�ѧ����ʽΪn CH2=CHCOOCH3$\stackrel{����}{��}$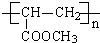
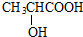 $\stackrel{����}{��}$
$\stackrel{����}{��}$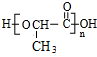 +��n-1��H2O
+��n-1��H2O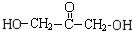 ��
��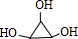 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
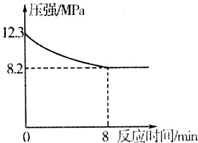 �о�̼���仯��������ʶ��ڿ��С��������������Ҫ���壮
�о�̼���仯��������ʶ��ڿ��С��������������Ҫ���壮�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com