
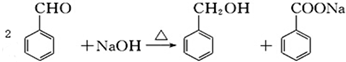
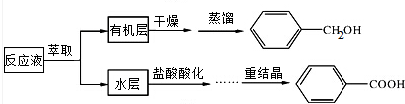
分析 反应液含有苯甲醇和苯甲酸钠,加入乙醚萃取,分液,得到的有机层为苯甲醇和乙醚的混合物,蒸馏可得到苯甲醇,水层为苯甲酸钠的水溶液,加入盐酸酸化得到苯甲酸,经蒸发结晶、过滤、洗涤可得到苯甲酸,
(1)根据苯甲醇易溶于乙醚,且乙醚与水互不相溶分析,加入盐酸可生成苯甲酸,经重结晶析出;
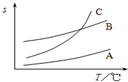
(2)应选择溶解度随温度变化较大的试剂,趁热过滤可除去杂质.
解答 解:反应液含有苯甲醇和苯甲酸钠,加入乙醚萃取,分液,得到的有机层为苯甲醇和乙醚的混合物,蒸馏可得到苯甲醇,水层为苯甲酸钠的水溶液,加入盐酸酸化得到苯甲酸,经蒸发结晶、过滤、洗涤可得到苯甲酸,
(1)苯甲醇易溶于乙醚,且乙醚与水互不相溶,可用乙醚作为萃取剂,分液时,应从下口放出下层液体,从上口倒出上层液体,加入盐酸可生成苯甲酸,经重结晶析出,
故答案为:乙醚;从下口放出下层液体,从上口倒出上层液体;将苯甲酸钠转化为苯甲酸,析出晶体;
(2)应选择试剂C,原因是在溶剂C中随温度变化苯甲酸的溶解度变化较大,有利于重结晶分离,分离时要趁热过滤,可除去不溶性杂质,防止苯甲酸冷却后结晶析出,洗涤时可用蒸馏水,防止引入其它杂质,
故答案为:C;除去不溶性杂质,防止苯甲酸冷却后结晶析出.
点评 本题考查物质的分离、提纯的实验设计,为高频考点,题目难度中等,试题侧重于学生实验设计和评价能力的考查,注意把握实验原理和实验基本操作方法,试题培养了学生的分析能力及化学实验能力.


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小苏打与盐酸反应 CO32-+2H+═H2O+CO2↑ | |
| B. | 向烧碱溶液中通入过量的CO2 CO2+2OH-═CO32-+H2O | |
| C. | 小粒钠投入冷水中 2Na+2H2O═2Na++2OH-+H2↑ | |
| D. | 用稀硝酸洗涤试管内壁的银镜:Ag+4H++3NO3-═Ag++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
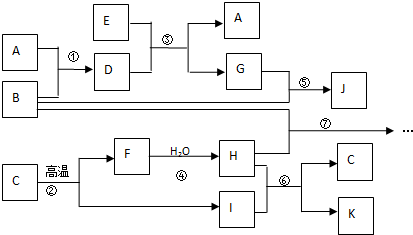
 ,化合物K的电子式为
,化合物K的电子式为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验内容 | 实验目的 | |
| A | 将AlCl3溶液蒸干灼烧 | 制备Al2O3 |
| B | 向淀粉水解后的溶液中,依次加入NaOH溶液、新制Cu(OH)2,共热 | 探究水解产物的还原性 |
| C | 向某溶液中加入稀硫酸,将产生的气体通入澄清石灰水 | 检验该溶液中是否含有CO32- |
| D | 向H2O2溶液中滴加少量FeCl3溶液 | 探究催化剂对化学反应速率的影响 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com