
| A、X、Y形成化合物表示为X2Y |
| B、X、Y形成的化合物中所含离子都是10电子微粒 |
| C、Y位于周期表中第ⅦA族,其最高正化合价为+7 |
| D、X原子半径小于Y的原子半径 |


科目:高中化学 来源: 题型:
| A、1mol O2所含的原子数目为NA |
| B、0.5mol H2O的质量为9g |
| C、16g CH4分子含有的电子数目为NA |
| D、标准状况下,11.2L氢气含有分子的物质的量是0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 ,请回答下列问题.
,请回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、反应物的总能量大于生成物的总能量 |
| B、该反应遵循“能量守恒定律” |
| C、该反应中,化学能只转变成热能 |
| D、断开1mol H-H键和1mol Cl-Cl键所吸收的总能量小于形成2mol H-Cl键所放出的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、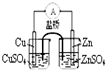 如图能组成Zn、Cu原电池 |
B、 如图能证明非金属性C>Si |
C、 如图说明反应2NO2?N2O4,△H>0 |
D、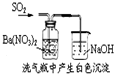 如图白色沉淀为BaSO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 操作、现象 | 解释或结论 |
| A.铝箔在酒精灯火焰上加热,熔化但不滴落 | 铝箔对熔化的铝有吸附作用 |
| B.向盛有0.005mol/L FeCl3溶液的试管中加入5mL 0.01mol/L KSCN溶液,溶液呈红色,再加入5滴饱和FeCl3溶液,红色加深 | 增大反应物的浓度,化学平衡向正反应方向移动 |
| C.向淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入新制的氢氧化铜悬浊液并加热,未见红色沉淀 | 淀粉未水解 |
| D.取某溶液少量,加入盐酸酸化的硝酸钡溶液,出现白色沉淀 | 该溶液中一定含有大量的SO42- |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com