
��ľ�������ܺ�K2CO3��K2SO4��NaCl���Σ�����ľ��������ˮ��ȡ�ý�ȡҺ����ʵ
�飬���и�������ó��Ľ�������ȷ����
A�����ȡҺ�м���BaCl2�а�ɫ������˵�����к���SO42��
B�����ȡҺ�м���AgNO3��Һ�а�ɫ������˵�����к���Cl��
C���ྻ�IJ�˿պȡ��ȡҺ�������ھƾ��ƻ��������գ�����ʻ�ɫ������ȷ���Ƿ�K+
D�����ȡҺ�еμ�ϡ���ᣬ������ɫ��ζ�����壬˵�����к���CO32��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������л���Ľṹ�������йص�������ȷ����(����)
A��������֬������ʹ����KMnO4��Һ��ɫ
B�������Cl2�ķ�Ӧ����ϩ��Br2�ķ�Ӧ����ͬһ���͵ķ�Ӧ
C�������ǡ����ǵķ���ʽ��ΪC6H12O6������Ϊͬ���칹��
D���Ҵ������������Na��Ӧ�ų�H2�����߷����й�������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ijͬѧ�����ˡ�84����Һ��˵���е��䷽������NaClO��������480 mL�� NaClO 25%���ܶ�Ϊ1.19 g/cm3������Һ������˵����ȷ����(����)
A������ҡ�Ⱥ���������Һ��������NaClO�����ʵ���Ũ��ƫС
B������ƿ������ˮϴ��������ɲ���������Һ������
C������õ�NaClO����Һ�ڿ����й��գ����ú���Һ��NaClO�����ʵ���Ũ�ȼ�С
D����Ҫ������NaClO���������Ϊ142.8 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
2014��5��������ѧ���о����֣��������������ӿ�����̼��������ˮ�γ�����ˮ�����ԭ�������ڿ�ȼ�����γɣ������о������ܽྻ��ȫ�ش�������������˵����ȷ����
A��̼������ˮ���ﴢ����������ѧ�仯
B��̼��������ʯ��Ϊͬ��������
C������ˮ�������ȼ����ͬһ����
D�������������ڵ�ˮ�����γɹ��ۼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ͼʾ�е���������W��X��Y��Z���ܰ���ͷ����һ��ת������
| W | X | Y | Z |
| |
| �� | Na | NaOH | Na2CO3 | NaCl | |
| �� | Al(OH)3 | Al2O3 | Al | NaAlO2 | |
| �� | SO2 | (NH4)2SO3 | NH4HSO3 | Na2SO3 | |
| �� | FeCl2 | Fe | FeSO4 | FeCl3 |
A���٢ڢۢܡ��� �� B���٢ڢۡ���������C���٢ۡ��� ����D���ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������������˹����塢���������ȷ�������ҪӦ�ã�ʵ������ȡ��������������֮һ�ǣ���һ�������0.3mol��L��1Al(NO3)3��Һ���ٵμӵ�2.0mol��L��1 (NH4)2CO3��Һ�У�����30min�����ˡ���ˮϴ�ӡ��Ҵ�ϴ�ӡ�������ո���ü�ʽ̼�����[��ѧʽ�ɱ�ʾΪ��(NH4)aAlb(OH)c(CO3)d]��Ȼ���ȷֽ�õ�������������
��1����ȡ����������ʱ���ٵμ�Al(NO3)3��Һ�����Ͻ��裬����ҪĿ����
��
��2��(NH4)aAlb(OH)c(CO3)d��a��b��c��d�Ĵ�����ϵʽΪ ��
��3��Ϊȷ����ʽ̼����淋���ɣ���������ʵ�飺
��ȷ��ȡ5.560g��Ʒ�����ܱ���ϵ�г�ּ��ȵ�300��ʹ����ȫ�ֽ��ҹ����������ٱ仯��
�ڲ�������̬��������ͨ������Ũ����ͼ�ʯ��װ�����գ���ʯ��װ������1.760g��
�����Ƶ�ʣ���������Ϊ2.040g��
��������ʵ�����ݼ����ʽ̼�������Ʒ�Ļ�ѧ��ɣ�д��������̣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ʵ������������������Ʊ��������������й����ʵ�����������±���
| ������ | ��Է������� | �ܶ�/g·cm-3 | �е�/�� | �ܽ��/100gˮ |
| ������ | 74 | 0.80 | 118.0 | 9 |
| ������ | 60 | 1.045 | 118.1 | ���� |
| ���������� | 116 | 0.882 | 126.1 | 0.7 |
��һ���������������Ʊ�
���ڸ����50mLԲ����ƿ�У�����13.5mL��������7.2mL�����ᣬ�ټ���3��4��Ũ���ᣬҡ�ȣ�Ͷ��1��2����ʯ��Ȼ��װ��ˮ��(���ã�ʵ������в��Ϸ����ȥ��Ӧ���ɵ�ˮ)���¶ȼƼ����������ܣ���������������Ӧ
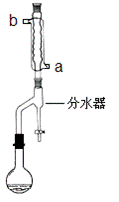
��������Ʒ�ľ���
�ڽ���ˮ���ֳ�������ͷ�ӦҺһ�����Һ©���У���10 mL��ˮϴ�ӡ��л��������10 mL10%Na2CO3ϴ�������ԣ�����10 mL ��ˮϴ�ӣ�����л���ת������ƿ�У�������ˮ����þ���
�۽���������������������50 mL ��ƿ�У���ѹ�����ռ�125��127 �����֣���11.6 g����������
��ش��й����⡣
��1����ˮӦ�ô������� ___________����a��b���ܿ�ͨ�롣
��2��������в��ϴӷ�ˮ���²��ֳ����ɵ�ˮ��Ŀ����_________________________
��������жϷ�Ӧ�յ��������_____________________________________��
��3����Ʒ�ľ��ƹ��̲�����У���һ��ˮϴ��Ŀ����_____________________________���ñ���Na2CO3��Һϴ���л��㣬�ò�������Ŀ����_________________________________��
��4�����й��ڷ�Һ©����ʹ��������ȷ����____
A����Һ©��ʹ��ǰ����Ҫ��©��ֻҪ��Һ©��������о����©ˮ����ʹ��
B��װҺʱ����Һ©����Һ�����������ó������ݻ���2/3
C����ȡ����Ӧ����ͼ��ʾ
D���ų�Һ��ʱ���轫��������ʹ���ϵİ��۶�©�����ϵ�С��
��5������۵ij�ѹ�������ռ�126�����֣��е����140����л������������һ�㲻�����������ܶ��ÿ��������ܣ�����ԭ����_________________________
��6����ʵ������У�����������������ʽ��116���IJ�����__________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij��ѧС������ͼ��ʾװ����ȡ����������˵����ȷ����(����)

A����װ��ͼ�����ٴ����������Դ���
B����ʵ�����ռ������ķ�������ȷ
C�������Ҫ�õ����﴿����Cl2��ֻ�������巢��װ�ú��ռ�װ��֮������һ��װ��Ũ�����ϴ��ƿ����
D������2 mol HCl��ijŨ����������MnO2��ϣ���һ�������·�Ӧ��ת��1 mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�弰�仯����㷺Ӧ����ҽҩ��ũҩ����ά��������ȼ���ȣ��ش��������⣺
��1����ˮ��������У���Ũ���ĺ�ˮ��ͨ�� �������е�Br-���������ÿ��������壻Ȼ����̼������Һ�����壬���绯ΪBr-��BrO3-�������ӷ���ʽΪ ��
��2�����������Թ��ۼ�����γ�BrCl��BrCl�����У� �������ԡ�BrCl��ˮ������Ӧ�Ļ�ѧ����ʽΪ ��
��3��CuBr2�ֽ���Ȼ�ѧ����ʽΪ��
2CuBr2(s)=2 CuBr(s)+ Br2(g) ��H=+105.4kJ/mol
���ܱ������н�����CuBr2��487K�¼��ȷֽ⣬ƽ��ʱp(Br2)Ϊ4.66��103Pa��
���練Ӧ��ϵ��������䣬��߷�Ӧ�¶ȣ���p(Br2)���� (����������䡱��С��)��
���練Ӧ�¶Ȳ��䣬����Ӧ��ϵ���������һ������p(Br2)�ı仯��ΧΪ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com