
 东晋《华阳国志•南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品.回答下列问题:
东晋《华阳国志•南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品.回答下列问题:分析 (1)Ni是28号元素,其原子核外有28个电子,根据构造原理书写镍元素基态原子的电子排布式;3d能级上的未成对的电子数为2;
(2)①[Ni(NH3)6]SO4中阴离子价层电子对个数=4+$\frac{6+2-4×2}{2}$=4且不含孤电子对,根据价层电子对互斥理论判断硫酸根离子的立体构型;
②含有孤电子对和含有空轨道的原子之间存在配位键,提供孤电子对的成键原子是N;
③有氢键的氢化物熔沸点较高;
氨气分子结构不对称,正负电荷重心不重合;氨气分子中中心原子N原子的价层电子对个数=3+$\frac{5-3×1}{2}$=4且含有一个孤电子对,根据价层电子对互斥理论判断N原子的轨道杂化类型;
(3)金属晶体中存在金属键;
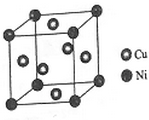
(4)①该晶胞中Ni原子个数=8×$\frac{1}{8}$=1、Cu原子个数=6×$\frac{1}{2}$=3;
②该晶胞的化学式为Cu3Ni,若合金的密度为dg/cm3,晶胞参数=$\root{3}{\frac{\frac{M}{{N}_{A}}}{ρ}}$.
解答 解:(1)Ni是28号元素,其原子核外有28个电子,根据构造原理书写镍元素基态原子的电子排布式为1s22s22p63s23p63d84s2或[Ar]3d84s2;3d能级上的未成对的电子数为2,
故答案为:1s22s22p63s23p63d84s2或[Ar]3d84s2;2;
(2)①[Ni(NH3)6]SO4中阴离子价层电子对个数=4+$\frac{6+2-4×2}{2}$=4且不含孤电子对,根据价层电子对互斥理论判断硫酸根离子的立体构型为正四面体,
故答案为:正四面体;
②含有孤电子对和含有空轨道的原子之间存在配位键,在[Ni(NH3)6]2+中Ni2+提供空轨道、NH3提供孤电子对,所以在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为配位键,提供孤电子对的成键原子是N,
故答案为:配位键;N;
③有氢键的氢化物熔沸点较高,氨气中含有氢键、膦中不含氢键,则氨的熔沸点高于膦;
氨气分子结构不对称,正负电荷重心不重合,所以为极性分子;氨气分子中中心原子N原子的价层电子对个数=3+$\frac{5-3×1}{2}$=4且含有一个孤电子对,根据价层电子对互斥理论判断N原子的轨道杂化类型为sp3,
故答案为:高于;氨气分子间存在氢键;极性;sp3;
(3)金属晶体中存在金属键,则该物质中含有金属键,故答案为:金属;
(4)①该晶胞中Ni原子个数=8×$\frac{1}{8}$=1、Cu原子个数=6×$\frac{1}{2}$=3,则Cu、Ni原子个数之比为3:1,故答案为:3:1;
②该晶胞的化学式为Cu3Ni,若合金的密度为dg/cm3,晶胞参数=$\root{3}{\frac{\frac{M}{{N}_{A}}}{ρ}}$=$\root{3}{\frac{\frac{251}{{N}_{A}}}{d}}$cm=$\root{3}{\frac{251}{d{N}_{A}}}$×107nm,故答案为:$\root{3}{\frac{251}{d{N}_{A}}}$×107.
点评 本题考查物质结构和性质,为高频考点,涉及晶胞计算、价层电子对互斥理论、配位键、原子核外电子排布等知识点,侧重考查学生对物质结构、基本理论的理解和运用,孤电子对的计算方法是易错点.


科目:高中化学 来源: 题型:解答题
| A | B | C | D | |
| A | -- | 白色沉淀 | 无现象 | 无色气体 |
| B | 白色沉淀 | -- | 白色沉淀 | 白色沉淀 |
| C | 无现象 | 白色沉淀 | -- | 无现象 |
| D | 无色气体 | 白色沉淀 | 无现象 | -- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
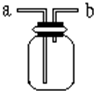 如图所示是中学化学实验中常见的装置,它有多种用途.
如图所示是中学化学实验中常见的装置,它有多种用途.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①②③⑥ | C. | ③⑥ | D. | ③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阳离子交换树脂 | B. | 阴离子交换树脂 | ||
| C. | 阳离子交换树脂和阴离子交换树脂 | D. | 离子交换树脂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -Y kJ/mol | B. | -(5X-0.5Y)kJ/mol | C. | -(10X-Y)kJ/mol | D. | +(10X-Y)kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com