
| A. | 用消毒液杀灭游泳池中的藻类 | |
| B. | 用CaCl2融化路面的积雪 | |
| C. | 用石灰修复被酸雨浸蚀的土壤 | |
| D. | 用催化剂将汽车尾气中的CO和NO转化为无害物质 |
分析 化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化学变化和物理变化的本质区别是否有新物质生成,据此分析判断.
解答 解:A.用消毒液杀灭游泳池中的藻类,过程中发生氧化还原反应说错了锌的物质属于化学变化,故A不符合;
B.融雪剂可以融化道路上的积雪.某种融雪剂由氯化钠和氯化钙组成,用CaCl2融化路面的积雪,氯盐类融雪剂溶于水(雪)后,溶液的冰点下降,都在零度以下.如氯化钠溶于水后冰点在-10℃,氯化钙在-20℃左右,醋酸盐类可达-30℃左右.盐的溶解使含盐雪水的凝固点降低,因此在雪水中溶解了盐之后就难以再形成冰块,无新物质生成,不是化学变化,故B符合;
C.二氧化硫与氮的氧化物能与水反应,生成硫酸、硝酸,溶液呈酸性,是造成酸雨的主要气体,在已酸化的土壤中加石灰,能改良酸性土壤,修复被酸雨浸蚀的土壤,故C不符合;
D.一氧化碳与一氧化氮发生氧化还原反应生成二氧化碳和氮气,所以利用催化措施,可以将汽车尾气中的CO和NO转化为无害气体,发生化学反应,故D不符合;
故选B.
点评 本题考查了很想知识的理解应用、物质性质的分析判断,注意知识积累,掌握基础是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 用湿润的红色石蕊试纸检验某种气体是否是NH3 | |
| B. | 某种有色溶液可使淀粉-KI试纸变蓝色,则该溶液中可能含有Fe3+ | |
| C. | 用玻璃棒蘸取溶液点在用蒸馏水湿润过的pH试纸上可测量该溶液的pH | |
| D. | 将湿润的蓝色石蕊试纸片粘在玻璃棒上置于氯气中,试纸先变红后褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.10 mol•L-1AgNO3溶液 | B. | 0.10 mol•L-1ZnSO4溶液 | ||
| C. | 0.20 mol•L-1CuCl2溶液 | D. | 0.20 mol•L-1Mg(NO3)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
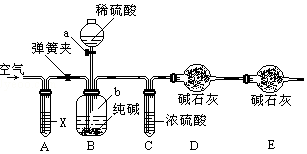 某纯碱样品中含有少量氯化钠杂质,现用如图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去).实验步骤如下:
某纯碱样品中含有少量氯化钠杂质,现用如图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去).实验步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 142g氯气中含Cl2的分子数为2NA | |
| B. | 1.7gOH-中所含电子的数目为NA | |
| C. | 49g硫酸中所含氧原子的数目为2NA | |
| D. | 71g硫酸钠中所含钠离子的数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.2gCH3OH含有的化学键数为0.4NA | |
| B. | 0.1molFeCl3水解制得的Fe(OH)3胶体中胶粒数是0.1NA | |
| C. | 标准状况下,2.24LCl2溶于足量水,转移的电子数为0.1NA | |
| D. | 0.2gD216O中含有的质子数、中子数和电子数均为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3和NaHCO3粉末与同浓度的盐酸时,Na2CO3因为碱性强,所以与盐酸反应放出气体速度快 | |
| B. | 等物质的量的两种盐与同浓度的盐酸反应,Na2CO3所消耗盐酸的体积是 NaHCO3的两倍 | |
| C. | 向Na2CO3饱和溶液中通人过量CO2,有NaHCO3结晶析出 | |
| D. | Na2CO3和NaHCO3溶液分别和BaCl2溶液反应,现象不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 原子半径:r(W)>r(Z)>r(Y) | |
| B. | 含Y元素的盐溶液一定显酸性 | |
| C. | 最高价氧化物对应水化物的酸性:Z>W | |
| D. | X、W分别形成的简单气态氢化物可反应生成离子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com