
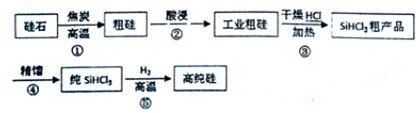
���� ��ʯ�ڸ�������̼������Ӧ�õ��ֹ裬�ֹ����Ҫ�ɷ�Ϊ�裬�ֹ辭����õ���ҵ�ֹ裬�ڸ���HCl��Χ�м��ȵõ�SiHCl3��Ȼ����õ�������SiHCl3���ڸ�������������Ӧ�����ɹ裬Ϊ�ߴ��裬��϶�Ӧ���ʵ������Լ���ĿҪ������⣮
��� �⣺��1��̼�Ͷ������跴Ӧ���ɹ裬̼��ԭ�������ã���ȡ�ߴ���ķ�Ӧ���������û����裬Ϊ�û���Ӧ���ʴ�Ϊ������ԭ�����û���Ӧ��
��2���ڷ�Ӧ���еõ��Ĵֹ躬����������̼�����ʣ������ᣬ�ɳ�ȥ�������Ƚ������ʣ��ʴ�Ϊ����ȥ�������Ƚ������ʣ�
��3������������ԭ��һ�����������û�����и���ֵķе㲻ͬ���ü��ȵķ�������ͬ�е����ʷ��룬�ʴ�Ϊ�����û�����и���ֵķе㲻ͬ���ü��ȵķ�������ͬ�е����ʷ��룻
��4����Ӧ��ΪSiO2+2C$\frac{\underline{\;����\;}}{\;}$Si+2CO����Ӧ��ΪSi+3HCl $\frac{\underline{\;\;��\;\;}}{\;}$SiHCl3+H2���ʴ�Ϊ��SiO2+2C$\frac{\underline{\;����\;}}{\;}$Si+2CO��Si+3HCl $\frac{\underline{\;\;��\;\;}}{\;}$SiHCl3+H2��
���� ���⿼�����Ʊ�ʵ�鷽����Ƶ��й�֪ʶ��Ϊ��Ƶ���㣬���ؿ����˹輰�仯������й�֪ʶ��ע��ֹ���ᴿ��Ӧԭ������Ŀ�Ѷ��еȣ���Ŀ����������ѧ���ķ���������ʵ��������


 �¿α�����Ķ�ѵ��ϵ�д�
�¿α�����Ķ�ѵ��ϵ�д� ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | -332 | B�� | +130 | C�� | +332 | D�� | -l30 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
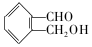 �ж���ͬ���칹�壬�������������Һ��б����ṹ�Ĺ��У�������
�ж���ͬ���칹�壬�������������Һ��б����ṹ�Ĺ��У�������| A�� | 7�� | B�� | 6�� | C�� | 5�� | D�� | 4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ȼ�������ȼ������SO3 | |
| B�� | �й��Ŵ�����������Һ���������ͭ�������ͭ�� | |
| C�� | ���ð�˾ƥ�ֳ���ˮ���ᷴӦʱ����NaHCO3��Һ�ⶾ | |
| D�� | ��������ֲ��ϲ������Ͻ���Ϊ���Ͻ�ǿ�ȴ������ᡢ����ʴ����ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ˮ | |
| B�� | �ɶ����ƶ��� | |
| C�� | һ��ƽ�й����䵰������Һʱ���Ӳ��濴�������ġ�ͨ·�� | |
| D�� | ��FeCl3��Һ�е���NaOH��Һ�����ֺ��ɫ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com