
| 元素 | 相关信息 |
| A | 在常温、常压下,其单质是气体,随着人类对环境的认识和要求的提高,它将成为备受青睐的清洁燃料 |
| B | 工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障 |
| C | 植物生长三要素之一,它能形成多种氧化物,其中一种是早期医疗中使用的麻醉剂 |
| D | 室温下其单质为淡黄色粉末状固体,加热易熔化.该单质在氧气中燃烧,发出明亮的蓝紫色火焰 |
| E | 它在地壳中储量丰富,是人体不可缺少的微量元素之一.其单质为银白色固体,是工农业生产中不可或缺的金属材料,常用于机械制备、建筑等行业 |
分析 I(1)将硫化钠溶液与氯化铝溶液混合,有白色沉淀和气体生成,但此沉淀不是硫化铝,是铝离子与硫离子发生沉淀双水解反应生成氢氧化铝与硫化氢;
(2)将NH3通过灼热的CuO,有无色无味的难溶于水的气体生成,该气体为N2,N元素发生氧化反应,则Cu元素发生还原反应生成Cu,同时生成水;
(3)反应生成黄绿色气体为Cl2,由电子守恒:n(Co3+)=2 n(Cl2)=2×$\frac{6.72L}{22.4L/mol}$=0.6 mol,由电荷守恒:n(Co原子)总=n(Co2+)溶液=$\frac{1}{2}$n(Cl-)=$\frac{1}{2}$×( 0.48L×5mol/L-2×0.3mol)=0.9 mol,所以固体中的n(Co2+)=0.9mol-0.6mol=0.3 mol,根据化合价代数和为0,氧化物中n(O)=(0.3mol×2+0.6mol×3)÷2=1.2mol,故该钴氧化物中n(Co):n(O)=0.9mol:1.2mol=3:4,故氧化物的化学式为Co3O4;
II.A在常温、常压下,其单质是气体,它将成为备受青睐的清洁燃,则A为H元素;工业上通过分离液态空气获得B单质,其某种同素异形体是保护地球地表环境的重要屏障,则B为O元素;C是植物生长三要素之一,它能形成多种氧化物,其中一种是早期医疗中使用的麻醉剂,则C为N元素;室温下D的单质为淡黄色粉末状固体,加热易熔化.该单质在氧气中燃烧,发出明亮的蓝紫色火焰,则D为S元素;E在地壳中储量丰富,是人体不可缺少的微量元素之一.其单质为银白色固体,是工农业生产中不可或缺的金属材料,常用于机械制备、建筑等行业,则E为Fe.
解答 解:I(1)将硫化钠溶液与氯化铝溶液混合,有白色沉淀和气体生成,但此沉淀不是硫化铝,是铝离子与硫离子发生沉淀双水解反应生成氢氧化铝与硫化氢,反应的离子方程式为:2Al3++3S2-+6H2O═2Al(OH)3↓+3H2S↑,
故答案为:2Al3++3S2-+6H2O═2Al(OH)3↓+3H2S↑;
(2)将NH3通过灼热的CuO,有无色无味的难溶于水的气体生成,该气体为N2,N元素发生氧化反应,则Cu元素发生还原反应生成Cu,同时生成水,反应的化学方程式为:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O,
故答案为:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O;
(3)反应生成黄绿色气体为Cl2,由电子守恒:n(Co3+)=2 n(Cl2)=2×$\frac{6.72L}{22.4L/mol}$=0.6 mol,由电荷守恒:n(Co原子)总=n(Co2+)溶液=$\frac{1}{2}$n(Cl-)=$\frac{1}{2}$×( 0.48L×5mol/L-2×0.3mol)=0.9 mol,所以固体中的n(Co2+)=0.9mol-0.6mol=0.3 mol,根据化合价代数和为0,氧化物中n(O)=(0.3mol×2+0.6mol×3)÷2=1.2mol,故该钴氧化物中n(Co):n(O)=0.9mol:1.2mol=3:4,故氧化物的化学式为:Co3O4,和盐酸反应的化学方程式为:Co3O4+8HCl═3CoCl2+Cl2↑+4H2O,
故答案为:Co3O4+8HCl═3CoCl2+Cl2↑+4H2O;
II.A在常温、常压下,其单质是气体,它将成为备受青睐的清洁燃,则A为H元素;工业上通过分离液态空气获得B单质,其某种同素异形体是保护地球地表环境的重要屏障,则B为O元素;C是植物生长三要素之一,它能形成多种氧化物,其中一种是早期医疗中使用的麻醉剂,则C为N元素;室温下D的单质为淡黄色粉末状固体,加热易熔化.该单质在氧气中燃烧,发出明亮的蓝紫色火焰,则D为S元素;E在地壳中储量丰富,是人体不可缺少的微量元素之一.其单质为银白色固体,是工农业生产中不可或缺的金属材料,常用于机械制备、建筑等行业,则E为Fe.
(4)N与H形成的某一化合物能和N与O形成的另一无色化合物(这两种化合物分子中原子个数比皆为1:2)一起用作火箭助推剂,分别为N2H4、N2O4,两者发生反应生成无毒物质,反应生成氮气与水,该反应化学反应方程式:2N2H4+N2O4═3N2+4H2O,
故答案为:2N2H4+N2O4═3N2+4H2O;
(5)化合物X是元素S的最高价氧化物的水化物,则X为H2SO4,在水中的电离方程为 H2SO4═2H++SO42-;常温下,Fe的单质与稀H2SO4反应生成盐Y为FeSO4.化合物Z仅由元素S和Fe组成,产物中n(H2SO4):n(FeSO4)=1:1,由元素守恒可知Z为FeS2,配平上述方程式:2FeS2+2H2O+7O2═2FeSO4+2H2SO4,
故答案为:H2SO4═2H++SO42-;FeSO4;2FeS2+2H2O+7O2═2FeSO4+2H2SO4;
(6)盐FeSO4受强热会发生分解反应,其气体产物由元素D(硫)的氧化物组成,设计实验验证其气体产物中所含元素D的氧化物的组成:将气体产物通入品红溶液,如果品红溶液褪色,则含有SO2,反之则无SO2.取适量吸收液于试管,滴加适量盐酸酸化,再滴加BaCl2,如有白色沉淀生成,则含有SO3,反之则无SO3,
故答案为:将气体产物通入品红溶液,如果品红溶液褪色,则含有SO2,反之则无SO2.取适量吸收液于试管,滴加适量盐酸酸化,再滴加BaCl2,如有白色沉淀生成,则含有SO3,反之则无SO3.
点评 本题考查结构性质位置关系综合应用、元素化合物知识、氧化还原反应、实验方案设计等,侧重分析与应用能力的考查,需要学生具备扎实的基础,难度中等.


科目:高中化学 来源: 题型:选择题
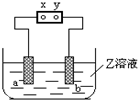 图中x、y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无臭气体放出,符合这一情况的( )
图中x、y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无臭气体放出,符合这一情况的( )| a极板 | b极析 | X电极 | Z溶液 | |
| A | 锌 | 石墨 | 负极 | CuSO4 |
| B | 石墨 | 石墨 | 负极 | NaOH |
| C | 银 | 铁 | 负极 | AgNO3 |
| D | 铜 | 石墨 | 负极 | CuCl2 |
| A. | A | B. | B | C. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水、易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
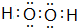 ,其中中心原子的杂化方式为sp3.
,其中中心原子的杂化方式为sp3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
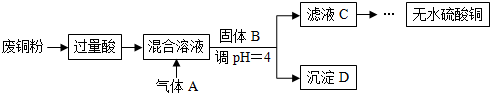
| A. | “过量酸”不适合用硝酸或浓硫酸,固体B可以用CuO、Cu(OH)2或Cu2(OH)2CO3 | |
| B. | 通入的气体A可以是O2或Cl2 | |
| C. | 通入气体A之前的混合溶液中存在的阳离子是:Fe2+、Cu2+、H+ | |
| D. | 将从溶液中得到的硫酸铜晶体在空气中加热,可制得无水硫酸铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨水 | B. | AgNO3 | C. | NaOH | D. | BaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Cu2+、NO3-、SO42-- | B. | K+、Na+、Cl-、SiO32- | ||
| C. | Al3+、NH4+、NO3-、Cl- | D. | K+、Na+、AlO2-、Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单离子半径:W>Y>X | |
| B. | Z与W形成的化合物在熔融状态下能导电 | |
| C. | 电解Y、W形成的化合物,无论是熔融状态下还是水溶液中,都能得到单质W | |
| D. | 单质X与单质Y加热条件下能生成白色固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com