
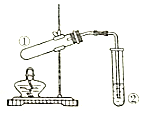
| 选项 | ①中试剂 | ②中溶液 | 实验目的 |
| A | 二氧化锰(s),浓盐酸 | 饱和食盐水 | 制取氯气 |
| B | Na2SO3(s),70%H2SO4 | 酸性高锰酸钾 | 验证SO2的还原性 |
| C | Na2CO3(s)或NaHCO3(s) | 澄清石灰水 | 鉴别Na2CO3和NaHCO3 |
| D | 乙醇、乙酸、浓硫酸 | 饱和碳酸钠 | 制取乙酸乙酯 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.图示装置中缺少收集氯气的装置;
B.亚硫酸钠与硫酸反应生成二氧化硫,可用酸性高锰酸钾溶液检验其还原性;
C.加热碳酸氢钠时,应该将大试管口稍稍向下倾斜;
D.吸收乙酸乙酯的导管不能插入溶液,否则会发生倒吸现象.
解答 解:A.制取氯气时,可用饱和食盐水除去氯气中含有的氯化氢,但图示装置中没有氯气的收集及尾气吸收装置,故A错误;
B.Na2SO3(s)与70%H2SO4反应生成的二氧化硫能够使酸性高锰酸钾溶液褪色,据此可证明二氧化硫的还原性,故B正确;
C.加热碳酸氢钠固体有水生成,大试管口必须稍稍向下倾斜,图示装置不合理,故C错误;
D.乙酸和乙醇在浓硫酸存在条件下加热可以生成乙酸乙酯,也可以用饱和碳酸钠溶液吸收乙酸乙酯,但吸收乙酸乙酯的导管不能伸入溶液中,否则易发生倒吸现象,故D错误;
故选B.
点评 本题考查了化学实验方案的评价,题目难度不大,明确常见物质制备原理及装置特点为解答关键,注意熟练掌握常见元素及其化合物性质,试题培养了学生的化学实验能力.


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Al3+、SO42-、NO3- | B. | K+、Fe2+、NO3-、SO42- | ||
| C. | K+、Cu2+、NH4+、Cl- | D. | Na+、K+、NO3-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用工业酒精配制饮用酒和调味用的料酒 | |
| B. | 食用白糖的主要成分是蔗糖 | |
| C. | 医用酒精的浓度通常为95% | |
| D. | 液化石油气的主要成分是甲烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 化学是一门以实验为基础的学科,化学实验是化学学习的重要内容.根据你掌握的知识判断,下列实验操作的描述中正确的是AC
化学是一门以实验为基础的学科,化学实验是化学学习的重要内容.根据你掌握的知识判断,下列实验操作的描述中正确的是AC查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①②③ | B. | 只有①②④ | C. | 只有①③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同温同压下,任何气体的分子间距离几乎相等 | |
| B. | 标准状况下,22.4LCCl4的物质的量是1mol | |
| C. | 等物质的量的N2和CO所含有的原子数均为2NA | |
| D. | 物质的量是科学上用来表示物质所含微粒质量的物理量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com