
| A. | 氧化剂和还原剂混合不一定发生氧化还原反应 | |
| B. | 得电子越多的氧化剂,其氧化性就越强 | |
| C. | 阳离子只有氧化性,阴离子只有还原性 | |
| D. | 有单质参加且有单质生成的反应一定属于氧化还原反应 |
分析 A.同种元素的相邻价态的物质不能发生氧化还原反应;
B.氧化性与得电子能力有关;
C.根据离子中某元素的化合价来分析其氧化性或还原性;
D.存在元素化合价变化的反应属于氧化还原反应.
解答 解:A.一般氧化剂、还原剂易发生氧化还原反应,但强氧化剂和强还原剂混合不一定发生氧化还原反应,如浓硫酸与二氧化硫不发生反应,故A正确;
B.氧化性与得电子能力有关,与得电子数目多少无关,故B错误;
C.最高价态的阳离子一般具有氧化性,如Fe3+;最低价的阴离子具有还原性,如I-;但Fe2+、SO32-都既有氧化性又有还原性,故C错误;
D.存在元素化合价变化的反应属于氧化还原反应,氧气转化为臭氧,有单质参加且有单质生成的反应不一定是氧化还原反应,故D错误.
故选A.
点评 本题考查氧化还原反应中氧化性、还原性、氧化、还原反应,学生应学会利用化合价来分析问题,并能举出常见的例子来解答此类习题,题目难度不大.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:解答题
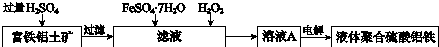
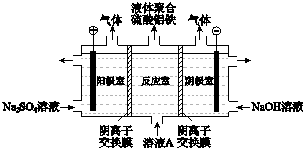 子交换膜只允许阴离子通过,电极为惰性电极)
子交换膜只允许阴离子通过,电极为惰性电极)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
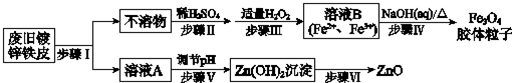
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl的摩尔质量是58.5g | |
| B. | 将40g氢氧化钠溶解在1L水中可配制物质的量浓度为1mol/L的氢氧化钠溶液 | |
| C. | 气体摩尔体积指lmol任何气体所占的体积约为22.4L | |
| D. | 10毫升1mol/L氯化铝溶液与50毫升3mol/L氯化钠溶液中所含氯离子物质的量浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 混合物 | 试剂 | 分离方法 | |
| A | 粗苯甲酸(泥沙等) | 水 | 重结晶 |
| B | 甲烷(乙烯) | 高锰酸钾酸性溶液 | 洗气 |
| C | 乙炔(硫化氢) | 硫酸铜溶液 | 洗气 |
| D | 溴苯(溴) | 稀氢氧化钠溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com