
һ�������£���3molA��1molB�����������ڹ̶��ݻ�Ϊ2L���ܱ������У��������·�Ӧ��3A(g)+B(g) 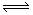 xC(g)+2D(s)��2minĩ�÷�Ӧ�ﵽƽ�⣬����0.8molD�������C��Ũ��Ϊ0.2mol/L�������ж���ȷ����( )
xC(g)+2D(s)��2minĩ�÷�Ӧ�ﵽƽ�⣬����0.8molD�������C��Ũ��Ϊ0.2mol/L�������ж���ȷ����( )
| A���������´˷�Ӧ�Ļ�ѧƽ�ⳣ��ԼΪ0.91 |
| B��A��ƽ����Ӧ����Ϊ0.3mol/(L��s) |
| C��B��ת����Ϊ60% |
| D�������������ܶȲ��ٸı�ʱ���÷�Ӧ��һ���ﵽƽ��״̬ |
A
�������������C��Ũ��Ϊ0.2mol?L?1������C�����ʵ���Ϊ0.4mol������x=1����������ʽ���㣺
3A(g)+ B(g) 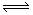 C(g)+2D(s)
C(g)+2D(s)
��ʼŨ�ȣ�mol?L?1�� 1.5 0.5 0
ת��Ũ�ȣ�mol?L?1�� 0.6 0.2 0.4
ƽ��Ũ�ȣ�mol?L?1�� 0.9 0.3 0.4
A���������´˷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ��0.4��(0.93��0.3)=0.91����ȷ��B��A��ƽ����Ӧ����=0.6mol/L��2min=0.3mol/(L��min)������C��B��ת����=0.2mol/L��0.5mol/L��100%=40%������D����Ϊ�������ݻ��̶�����DΪ���壬��Ӧǰ������������仯�����������������ܶȲ��ٸı�ʱ���÷�Ӧһ���ﵽƽ��״̬������
���㣺���⿼�黯ѧƽ����жϡ�ƽ�ⳣ���뷴Ӧ���ʵļ��㡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ס��ҡ��������ܱ������г���һ������A��B��������Ӧ��A(g)+xB(g) 2C(g)���������ķ�Ӧ�¶ȡ���Ӧ����ʼ������Ӧ������C��Ũ����ʱ��仯��ϵ�ֱ�����ͼ���±���ʾ������˵����ȷ����
2C(g)���������ķ�Ӧ�¶ȡ���Ӧ����ʼ������Ӧ������C��Ũ����ʱ��仯��ϵ�ֱ�����ͼ���±���ʾ������˵����ȷ����
| ���� | �� | �� | �� |
| �ݻ� | 0.5L | 0.5L | 1.0L |
| �¶�/�� | T1 | T2 | T2 |
| ��Ӧ�� ��ʼ�� | 1.5molA 0.5molB | 1.5molA 0.5molB | 6.0molA 2.0molB |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ij�ܱ������г�������ʵ���������A��B��һ���¶��·�����ӦA(g)��xB(g) 2C(g)���ﵽƽ���ֻ�ı䷴Ӧ��һ����������������и����ʵ�Ũ�ȡ���Ӧ������ʱ��仯�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����
2C(g)���ﵽƽ���ֻ�ı䷴Ӧ��һ����������������и����ʵ�Ũ�ȡ���Ӧ������ʱ��仯�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����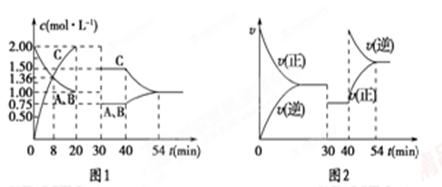
| A��30 minʱ�ı�������ǽ����¶ȣ�40 minʱ�ı�������������¶� |
| B��8 minǰA��ƽ����Ӧ����Ϊ0.08 mol/(L��min) |
| C����Ӧ�Ļ�ѧ����ʽ�е�x��1��������ӦΪ���ȷ�Ӧ |
| D��20 min��÷�Ӧ��ƽ�ⳣ����Ϊ4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪��Ӧ��CO(g)��CuO(s)  CO2(g)��Cu(s)�ͷ�Ӧ��H2(g)��CuO(s)
CO2(g)��Cu(s)�ͷ�Ӧ��H2(g)��CuO(s) Cu(s)��H2O(g)����ͬ��ij�¶��µ�ƽ�ⳣ���ֱ�ΪK1��K2�����¶��·�Ӧ��CO(g)��H2O(g)
Cu(s)��H2O(g)����ͬ��ij�¶��µ�ƽ�ⳣ���ֱ�ΪK1��K2�����¶��·�Ӧ��CO(g)��H2O(g) CO2(g)��H2(g)��ƽ�ⳣ��ΪK��������˵����ȷ����
CO2(g)��H2(g)��ƽ�ⳣ��ΪK��������˵����ȷ����
| A����Ӧ�ٵ�ƽ�ⳣ�� |
B����Ӧ�۵�ƽ�ⳣK��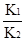 |
| C�����ڷ�Ӧ�ۣ�����ʱ���¶����ߣ�H2Ũ�ȼ�С����÷�Ӧ���ʱ�Ϊ��ֵ |
| D�����ڷ�Ӧ�ۣ����º����£�����ѹǿ��H2Ũ��һ����С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�Կ��淴Ӧ4NH3��g��+ 5O2��g�� 4NO��g��+ 6H2O��g��������������ȷ���ǣ� ��
4NO��g��+ 6H2O��g��������������ȷ���ǣ� ��
| A���ﵽ��ѧƽ��ʱ��4������O2��= 5������NO�� |
| B������λʱ��������x mol NO��ͬʱ������x mol NH3 ����Ӧ�ﵽƽ��״̬ |
| C���ﵽ��ѧƽ��ʱ�����������������������Ӧ���ʼ��٣��淴Ӧ�������� |
| D����ѧ��Ӧ���ʹ�ϵ�ǣ�2������NH3��= 3������H2O�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����������ɵ����ϳɰ����ķ��������1918��ŵ������ѧ��������һ�ܱ������г���1molN2��3molH2����һ�������·�����ӦN2��3H2 2NH3 �������й�˵����ȷ���ǣ�
2NH3 �������й�˵����ȷ���ǣ�
| A���ﵽ��ѧƽ��ʱ��N2����ȫת��ΪNH3 |
| B���ﵽ��ѧƽ��ʱ��N2��H2��NH3�����ʵ���Ũ�Ȳ��ٱ仯 |
| C���ﵽ��ѧƽ��ʱ����Ӧ��ֹͣ���� |
| D������Ӧ�ﵽƽ��ʱ��ÿ��3mol��H��H���ѣ�ͬʱ����6mol��N��H�����ѡ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪��ӦA(g)��3B(g)=2C(g)��D(g)��ij��ʱ������A��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧ����Ϊ1 mol/(L��min)����˶�ʱ������C��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧ����Ϊ�� ��
| A��0.5 mol/(L��min) | B��1 mol/(L��min) |
| C��2 mol/(L��min) | D��3 mol/(L��min) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�跴Ӧ��Fe(s)��CO2(g)  FeO(s)��CO(g) ��H��a kJ/mol����Ӧ��Fe(s)��H2O(g)
FeO(s)��CO(g) ��H��a kJ/mol����Ӧ��Fe(s)��H2O(g)  FeO(s)��H2(g) ��H��b kJ/mol����������Ӧ��ƽ�ⳣ���ֱ�ΪK1��K2���ڲ�ͬ�¶��£�K1��K2��ֵ���£�
FeO(s)��H2(g) ��H��b kJ/mol����������Ӧ��ƽ�ⳣ���ֱ�ΪK1��K2���ڲ�ͬ�¶��£�K1��K2��ֵ���£�
| T/K | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1 173 | 2.15 | 1.67 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���淴ӦmA(g)��nB pC(g)��qD(����A��C������ɫ����)�����ﵽƽ��ʱ������������ȷ����(����)
pC(g)��qD(����A��C������ɫ����)�����ﵽƽ��ʱ������������ȷ����(����)
A������ѹǿ��ƽ�ⲻ�ƶ���˵��(m��n)һ������(p��q)
B�������¶ȣ�A��ת���ʼ�С��˵������Ӧ�����ȷ�Ӧ
C��������B������ƽ����ϵ��ɫ���˵��B������������
D����B�����壬����A������A��Bת���ʶ�һ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com