
【题目】某同学用如图所示装置探究原电池的工作原理,并推出下列结论,其中不正确的是( )
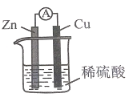
A.锌片不断溶解,说明Zn失去电子
B.铜片上产生气泡,说明溶液中H+在其表面得到电子
C.电流计指针发生偏转,说明该装置将电能转换为化学能
D.该装置中发生的总反应为Zn+H2SO4=ZnSO4+H2↑
科目:高中化学 来源: 题型:
【题目】原子序数由小到大排列的五种短周期元素X、Y、Z、M、W,其中X是在周期表中原子半径最小的元素,Z 的最外层电子数是内层的3倍,Y、Z左右相邻,Z、W位于同主族,M与W同周期,且与X同主族。
(1)M元素是_______(填元素符号)。
(2)Z、W形成的气态氢化物中,较稳定的是_______(填化学式)。
(3)写出M2Z2的电子式:_______。
(4)由X、Y、Z、W四种元素中的三种组成的一种强酸,其稀溶液能与铜反应,离子方程式为_______。
(5)由X、Y、Z、W四种元素组成的一种离子化合物A,已知:
①1molA能与足量NaOH热的浓溶液反应生成标准状况下44.8L气体;
②A能与盐酸反应产生气体B,该气体能使品红溶液退色。
写出①中反应的化学方程式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种极易溶于水且几乎不与冷水反应的黄绿色气体(沸点11℃),实验室制备纯净ClO2溶液的装置如图所示:

已知下列反应:NaClO3+HCl→NaCl+ClO2+Cl2+H2O;NaClO2+HCl→NaCl+ClO2+H2O;NaClO2+Cl2→NaCl+ClO2(均未配平)。下列说法正确的是
A.a中通入的N2可用CO2或SO2代替B.b中NaClO2可用饱和食盐水代替
C.c中广口瓶最好放在冰水浴中冷却D.d中吸收尾气后只生成一种溶质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列填空:
(1)写出下列物质在水溶液中的电离方程式:①H2CO3:_______;②NaHCO3:___________。
(2)完成下列反应的离子方程式:①向NaHSO3溶液中加入过量NaHSO4溶液__;②小苏打溶液与乙酸溶液混合___;③FeBr2溶液中通入过量Cl2:____。
(3)25 ℃时,下列各组离子在指定溶液中一定能大量共存的是(______)
A.无色溶液中:Na+、NH4+、Cu2+、SO42-
B.0.1 mol·L-1的NH4HCO3溶液中:K+、SiO32-、AlO2-、Cl-
C.25 ℃时,Kw/c(H+)=1×10-2 mol·L-1的溶液中:K+、NO3-、S2-、ClO-
D.使甲基橙呈红色的溶液中:NH4+、Ba2+、Al3+、Cl-
(4)200 mL某溶液中有5种离子大量共存,其中4种离子的物质的量如下表:
离子 | H+ | K+ | NO3- | SO42- |
物质的量(mol) | 0.5 | 0.1 | 0.6 | 0.15 |
则另外一种离子是________(填写代号),该离子的浓度为________。
A.Fe2+ B.Cl- C.Al3+ D.ClO-
查看答案和解析>>
科目:高中化学 来源: 题型:
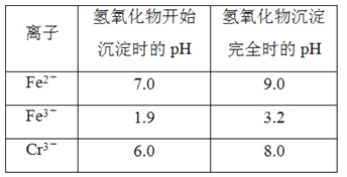
【题目】欲降低废水中重金属元素铬的毒性,可将Cr2O![]() 转化为Cr(OH)3沉淀除去。已知该条件下:
转化为Cr(OH)3沉淀除去。已知该条件下:
(1)某含铬废水处理的主要流程如图所示:
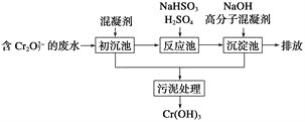
①初沉池中加入的混凝剂是K2SO4·Al2(SO4)3·2H2O,其作用为(用离子方程式表示)____。
②反应池中发生主要反应的离子方程式是Cr2O72-+3HSO3-+5H+===2Cr3++3SO42-+4H2O。根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子方程式是_____、____。证明Cr3+沉淀完全的方法是____。
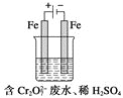
(2)工业可用电解法来处理含Cr2O![]() 废水。实验室利用如图装置模拟处理含Cr2O72-的废水,阳极反应式是Fe-2e-===Fe2+,阴极反应式是2H++2e-===H2↑。Fe2+与酸性溶液中的Cr2O72-反应的离子方程式是_____,得到的金属阳离子在阴极区可沉淀完全。用电解法处理该溶液中0.01molCr2O72-时,至少得到沉淀的质量是____g。
废水。实验室利用如图装置模拟处理含Cr2O72-的废水,阳极反应式是Fe-2e-===Fe2+,阴极反应式是2H++2e-===H2↑。Fe2+与酸性溶液中的Cr2O72-反应的离子方程式是_____,得到的金属阳离子在阴极区可沉淀完全。用电解法处理该溶液中0.01molCr2O72-时,至少得到沉淀的质量是____g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的Na、Na2O、Na2O2的混合物与足量的水反应,在标准状况下得到a L混合气体。将该混合气体通过电火花引燃,恰好完全反应,则原混合物中Na、Na2O、Na2O2的物质的量之比可能为
A. 2:1:1
B. 1:1:2
C. 1:2:1
D. 4:3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在密闭恒容容器中,能表示反应X(g)+2Y(g)![]() 2Z(g)一定达到化学平衡状态的是( )
2Z(g)一定达到化学平衡状态的是( )
①X、Y、Z的密度不再发生变化 ②v正(Y)= 2v逆(X) ③容器中的压强不再发生变化 ④单位时间内生成nmol Z,同时生成2nmolY
A. ①② B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素化合物在生产生活中有很多应用,写出与下列应用相关的化学方程式 。
(1)漂白粉生效原理______________________________________________
(2)粗硅的制取___________________________________________________
(3)过氧化氢氧化碘离子___________________________________________
(4)实验室制取氨气_______________________________________________
(5)过量二氧化硫与澄清石灰水反应_____________________________________________
(6)氯碱工业生产氯气_____________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA,下列说法正确的是
A. 标准状况下,2.24LCH3OH分子中共价键的数目为0.5NA
B. 1 L1 mol·L-1HCl溶液中含有NA个HCl分子
C. 12.0 g熔融的NaHSO4中含有的阳离子数为0.1NA
D. 1mol SO2与足量O2在一定条件下充分反应生成SO3,共转移2 NA个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com