
科目:高中化学 来源:不详 题型:单选题
| A.X的氢化物溶于水显酸性 |
| B.Y的氧化物是离子化合物 |
| C.X与Y形成化合物的化学式为YX |
| D.X和Z的最高价氧化物对应的水化物都是弱酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
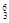 Li 、②
Li 、②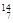 N 、③
N 、③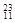 Na 、④
Na 、④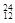 Mg 、⑤
Mg 、⑤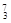 Li 、⑥
Li 、⑥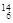 C 、⑦C60 、⑧石墨中,选择序号填空。
C 、⑦C60 、⑧石墨中,选择序号填空。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.有机化合物在空气中都可燃烧 |
| B.同周期元素的第一电离能(I1)从左到右依次增大 |
| C.分子晶体的熔点一定比金属单质的熔点低 |
| D.浓硝酸的还原产物是NO2,稀硝酸的氮元素可被还原为更低价态,但浓硝酸的氧化性比稀硝酸强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| V | 420 | 3100 | 4400 | 5900 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
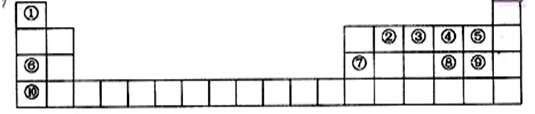
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Y是第三周期ⅦA族元素 | B.Z一定是金属元素 |
| C.非金属性:W﹥X | D.Y与W的最高正价之和为8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com