
W、X、Y、Z四种短周期主族元素的原子序数依次增大,W、X原子的最外层电子数之比为4:3,Z原子比X原子的核外电子数多4。下列说法正确的是
| A.W、Y、Z的电负性大小顺序一定是Z>Y>W |
| B.W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z |
| C.Y、Z形成的分子的空间构型可能是正四面体 |
| D.WY2分子中δ键与π键的数目之比是2:1 |
C
解析试题分析:短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,由于最外层电子数不超过8,故W的最外层电子数为4,处于第ⅣA族,X的最外层电子数为3,处于第ⅢA族,原子序数X大于W,故W为C元素,X为Al元素,Z原子比X原子的核外电子数多4,故Z的核外电子数为17,则Z为Cl元素,Y的原子序数大于铝元素,小于氯元素,故Y为Si或P或S元素,A、同主族自上而下电负性减弱,Y若为Si元素,则电负性C>Si,故A错误;B、同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径Al>Y>Cl>C,故B错误;C、若Y、Z形成的分子为SiCl4,为正四面体构型,故C正确;D、WY2分子为CS2,分子结构式为S=C=S,双键中含有1个δ键、1个π键,故δ键与π键的数目之比1:1,故D错误;
考点:考查结构性质位置关系的相关知识点,。


科目:高中化学 来源: 题型:填空题
根据要求完成下列各小题
(1)①实验室用加热固体混合物的方法制备氨气的化学反应方程式是 。
②为了得到干燥的NH3,用________做干燥剂。(填编号)
| A.碱石灰 | B.浓H2SO4 | C.无水CaCl2 | D.P2O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
物质X、Y、Z均含同种短周期元素,其转化关系如下图所示(反应条件未标出)。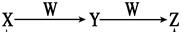
(1)若X是无色极易溶于水的刺激性气味气体,Z是红棕色气体,由Y与W反应生成Z的化学方程式是_______________________________________________________。
(2)若X含三种短周期元素,其中两种元素的原子的质子数之和等于另一种元素原子的质子数,单质W是常见金属,则X的稀溶液转化为Y的离子方程式是
。
(3)若X是空气的主要成分之一,W原子的最外层电子数是内层电子数的二倍;则Y与W反应生成0.1 mol Z时,反应中转移的电子数为__________________________。
(4)若Y是白色胶状沉淀,W为烧碱,则0.1mol Y与足量W反应生成Z时消耗烧碱的质量为 克 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关叙述正确的是( )
A. O和 O和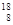 O中子数相同,质子数不同,互为同位素 O中子数相同,质子数不同,互为同位素 |
| B.H2O比H2S稳定,H—S键比H—O键更难断裂 |
| C.Na2O晶体中存在离子键,是离子化合物 |
| D.Na2O2晶体中阳离子与阴离子个数比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列大小比较正确的是
| A.离子半径:Na+>Mg2+>Al3+>Cl—;原子半径:Na>Mg>Al>Cl |
| B.稳定性:HF>H2O>NH3>CH4; 还原性: HF < H2O < NH3< CH4 |
| C.碱性:CsOH>KOH>Mg(OH)2>NaOH ; 金属性:Cs>K>Mg>Na |
| D.酸性:HClO>H2SO4>H2CO3;非金属性Cl>S>C |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在短周期中,R原子最外层电子数是其次外层电子数的3倍,下列说法不正确的是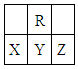
| A.原子半径大小:X >Y>Z |
| B.氢化物的稳定性:X >Y |
| C.化合物YR2能使品红溶液褪色 |
| D.X、Y、Z三种元素最高价氧化物的水化物的酸性最强的是Z |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
XY2是由短周期元素形成的化合物,Y-比X2+多一个电子层,且与氩原子的电子层结构相同。下列有关叙述不正确的是( )
| A.X是第二周期元素 | B.Y是第ⅦA族元素 |
| C.Y-与X2+的最外层电子数相同 | D.化合物XY2的化学键为离子键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com