
化合物A最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯、玉米淀粉等发酵制得。A的钙盐是人们喜爱的补钙剂之一。A在某种催化剂存在下进行氧化,其产物不能发生银镜反应。在浓硫酸存在下,A可发生如下图所示的反应:
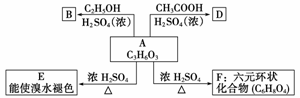
试写出:
化合物的结构简式:
A__________________,B________________________________________________________________________,
D__________________。
化学方程式:A→E:
________________________________________________________________________
________________________________________________________________________,
A→F:________________________________________________________________________。
科目:高中化学 来源: 题型:
下列除去括号内杂质的有关操作方法不正确的是
A.淀粉溶液(葡萄糖):渗析
B.乙醇(乙酸):加KOH溶液,分液
C.甲醇溶液(甲酸):加NaOH溶液,蒸馏
D.肥皂液(甘油):加食盐搅拌、盐析、过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
紫杉醇是一种新型抗癌药,其分子式为C47H51NO14,它是由如下的A酸与B醇生成的一种酯。
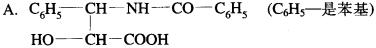
B.R-OH(R是一个含C、H、O的基团)
(1)A可在无机酸催化下水解,其反应方程式是
____ _____。
(2)A水解所得的氨基酸不是天然蛋白质水解产物,因为氨基酸不在(填希腊字母)_ 位。
(3)写出R-OH的分子式_ ____。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质不属于同分异构体的是( )
A.2,2二甲基丙醇和2甲基丁醇
B.邻氯甲苯和对氯甲苯
C.2甲基丁烷和戊烷
D.甲基丙烯酸和甲酸丙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关烯烃的说法中,正确的是( )
A.烯烃分子中所有的原子一定在同一平面上
B.烯烃在适宜的条件下只能发生加成反应,不能发生取代反应
C.分子式是C4H8的烃分子中一定含有碳碳双键
D.烯烃既能使溴水褪色也能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率v(纵坐标)与反应时间t(横坐标)的关系如图所示,已知该反应速率随着溶液中[H+]的增大而加快。
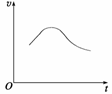
反应开始时反应速率加快的原因是
________________________________________________________________________
________________________________________________________________________
________________;
反应后期反应速率减慢的原因是
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某铝合金(硬铝)中含有镁、铜、硅,为了测定该合金中铝的含量,有人设计如下实验:
(1)取样品a g,称取时使用的仪器名称为托盘天平.
(2)将样品溶于足量稀盐酸中,过滤,滤渣中含有;在溶解过滤时使用的主要仪器有
(3)往滤液中加入过量溶液,过滤,写出该步操作中有关的化学方程式:.
(4)在第(3)步的滤液中通入足量CO2,过滤,将沉淀用蒸馏水洗涤数次后,烘干并灼烧至重量不再减少为止,冷却后称量,质量为b g.有关反应的化学方程式为:.
(5)计算该样品中铝的质量分数的表达×100%.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com