
| 1 |
| 4 |

| 1 |
| 4 |
| 1 |
| 4 |
| c2(CO)?c2(H2) |
| c(CH4)?c(CO2) |
| 12×12 |
| 1×1 |
| 2 |
| 6 |


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
| A、Na和O2 |
| B、NaOH溶液和CO2 |
| C、Na2O2和CO2 |
| D、AlCl3溶液和NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
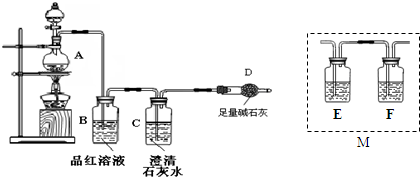
查看答案和解析>>
科目:高中化学 来源: 题型:
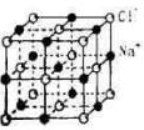
| A、一个金刚石的晶胞中有8个C原子 |
| B、金刚石的密度为3.54g?cm-1 |
| C、在该种CO2晶体中,一个CO2分子由一个C原子和二个氧原子构成 |
| D、在该种CO2晶胞中含氧原子8个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、BaSO4的溶度积常数比BaCO3的小 |
| B、SO42-没有毒性CO32-有毒性 |
| C、BaSO4密度大 |
| D、胃酸能与CO32-结合,生成CO2和H2O,使BaCO3的沉淀溶解平衡向右移动,使Ba2+浓度增大,造成中毒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com