
【题目】甲烷是一种重要的化工原料和清洁能源,研究其再生及合理利用有重要意义。
请回答:
(1)已知一定条件下发生如下反应:
CO2(g)+2H2O(g)![]() CH4(g)+2O2(g) △H=+802kJ·mol-1。
CH4(g)+2O2(g) △H=+802kJ·mol-1。
将一定量的CO2(g)和H2O(g)充入10L密闭容器中,分别在催化剂M、N的作用下发生上述反应,CH4(g)的产量(n)与光照时间(t)和温度(T)变化的关系如图1所示。
①若甲烷的燃烧热(△H)为-890kJ·mol-1,则水的汽化热△H=___________。(汽化热指1mol液体转化为气体时吸收的热量)
②T1℃、催化剂M作用下,0~20h内该反应速率v(H2O)=___________。

③根据图1判断,T1___________T2(填“>”“<”或“=”),理由为___________。
催化剂的催化效果:M___________N(填“强于”或“弱于”)。
(2)甲烷可用于制备合成气:CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H。将CH4(g)和H2O(g)以物质的量之比为1:3充入盛有催化剂的刚性容器中发生该反应。相同时间段内测得CO的体积分数(
CO(g)+3H2(g) △H。将CH4(g)和H2O(g)以物质的量之比为1:3充入盛有催化剂的刚性容器中发生该反应。相同时间段内测得CO的体积分数(![]() )与温度(T)的关系如图2所示。
)与温度(T)的关系如图2所示。
①T0℃时,CO的体积分数最大的原因为_________________________________。
②若T0℃时,容器内起始压强为p0,CO的平衡体积分数为10%,则反应的平衡常数Kp=___________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
【答案】+44 kJmol﹣1 0.006 molL﹣1h﹣1 > 该反应为吸热反应,温度升高,CH4的产量增大 弱于 低于T0 ℃时,相同时间段内温度越高反应速率越快,CO的体积分数越大;高于T0 ℃时,反应达到平衡,该反应为放热反应,温度越高CO的体积分数越小 ![]()
【解析】
(1)甲烷的燃烧热为△H=-890kJmol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890kJmol-1,根据盖斯定律,结合已知热化学方程式处理得H2O(l)=H2O(g),再计算出△H;
②根据图象可知,T1℃、催化剂M作用下,0~20h内甲烷的物质的量变化为0.6mol,结合v=![]() 计算出甲烷的反应速率,然后结合反应速率与化学计量数成正比计算;
计算出甲烷的反应速率,然后结合反应速率与化学计量数成正比计算;
③根据催化剂不影响平衡,会使得化学反应速率增大,结合该反应为放热反应分析解答;
(2)①没有达到平衡状态时,温度越高反应速率越快,当达到平衡状态后,升高温度平衡向着逆向移动,据此分析;
②CH4(g)和H2O(g)的物质的量之比为1∶3,设CH4为xmol,H2O为3xmol,平衡时生成的CO为ymol,然后根据三段式分析解答。容器容积相同时,气体的压强与物质的量成正比,T0℃时,容器内起始压强为p0,计算出平衡时的压强,再分别计算出平衡时各气体的分压,带入平衡常数表达式计算即可。
(1)①已知:CO2(g)+2H2O(g)CH4(g)+2O2(g)△H=+802kJmol﹣1①,甲烷的燃烧热为△H=﹣890kJmol﹣1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=﹣890 kJmol﹣1②,根据盖斯定律,﹣![]() (①+②)可得:H2O(l)=H2O(g)△H=﹣
(①+②)可得:H2O(l)=H2O(g)△H=﹣![]() [+802kJmol﹣1+(﹣890 kJmol﹣1)]=+44 kJmol﹣1,故答案为:+44 kJmol﹣1;
[+802kJmol﹣1+(﹣890 kJmol﹣1)]=+44 kJmol﹣1,故答案为:+44 kJmol﹣1;
②根据图像可知,T1℃、催化剂M作用下,0~20h内水的物质的量变化为0.6mol,则v(CH4)=0.003 molL﹣1h﹣1,所以v(H2O)=2v(CH4)=0.006 molL﹣1h﹣1,故答案为:0.006 molL﹣1h﹣1;
③该反应为吸热反应,温度升高,CH4的产量增大,根据图像可知,温度为T1条件下,平衡时甲烷的物质的量较大,则T1>T2;已知温度T1>T2,若不使用催化剂,应该在温度T1条件下优先达到平衡状态,根据图像可知,使用催化剂N的曲线优先达到平衡状态,说明催化剂的催化效果:M弱于N,故答案为:>;该反应为吸热反应,温度升高,CH4的产量增大;弱于;
(2)①在温度低于T0 ℃时,相同时间段内温度越高反应速率越快,则CO的体积分数越大;在温度为T0 ℃时,反应达到平衡,由于该反应为放热反应,温度越高CO的体积分数越小,所以T0℃时CO的体积分数最大,故答案为:低于T0 ℃时,相同时间段内温度越高反应速率越快,CO的体积分数越大;高于T0 ℃时,反应达到平衡,该反应为放热反应,温度越高CO的体积分数越小;
②CH4(g)和H2O(g)的物质的量之比为1∶3,设CH4为xmol,H2O为3xmol,平衡时生成的CO为ymol,CO的平衡体积分数为10%
CH4(g)+H2O(g)CO(g)+3H2(g)
初始(mol) x 3x 0 0
转化(mol) y y y 3y
平衡(mol) x﹣y 3x﹣y y 3y
则:![]() ×100%=10%,解得:y=0.5x,平衡时混合气体的总物质的量为:x-0.5x+3x-0.5x+0.5x+0.5x×3=5x,反应前总物质的量为4xmol,容器容积相同时,气体的压强与物质的量成正比,T0℃时,容器内起始压强为p0,则平衡时压强为:p0×
×100%=10%,解得:y=0.5x,平衡时混合气体的总物质的量为:x-0.5x+3x-0.5x+0.5x+0.5x×3=5x,反应前总物质的量为4xmol,容器容积相同时,气体的压强与物质的量成正比,T0℃时,容器内起始压强为p0,则平衡时压强为:p0×![]() =1.25p0,平衡时/span>p(CH4)=
=1.25p0,平衡时/span>p(CH4)=![]() ×1.25p0=
×1.25p0=![]() p0,p(H2O)=
p0,p(H2O)=![]() ×1.25p0=
×1.25p0=![]() p0,p(CO)=
p0,p(CO)=![]() ×1.25p0=
×1.25p0=![]() p0,p(CH4)=
p0,p(CH4)=![]() ×1.25p0=
×1.25p0=![]() p0,反应的平衡常数Kp=
p0,反应的平衡常数Kp= =
=![]() ,故答案为:
,故答案为:![]() 。
。


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】现有如下各种说法:
①金属和非金属化合时一定形成离子键;
②离子键是阳离子、阴离子的相互吸引力;
③根据电离方程式HCl![]() H++Cl-,判断氯化氢分子里存在离子键;
H++Cl-,判断氯化氢分子里存在离子键;
④氢气和氯气的反应过程:H2、Cl2分子里共价键发生断裂生成H原子、Cl原子,而后H原子、Cl原子形成离子键的过程
上述各种说法正确的是
A. ①② B. 都不正确 C. ①②④ D. ①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,对于可逆反应:X(g)+3Y(g) ![]() 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol ·L-1,则下列判断正确的是( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol ·L-1,则下列判断正确的是( )
A. c1∶c2=1∶3
B. 平衡时Y和Z的生成速率之比为2∶3
C. X、Y的转化率之比为1:3
D. c1的取值范围为0.04 mol·L-1<c1<0.14 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是 ( )
A. FeCl3溶液、Fe(OH)3胶体与Fe(OH)3沉淀的本质区别是有没有丁达尔效应
B. 根据分散系的稳定性大小将混合物分为胶体、溶液和浊液
C. 将几滴汽油加入装有10mL水的试管中,用力振荡形成胶体
D. 胶体、分散系、混合物概念间的从属关系可用图表示

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种元素,A元素的原子得两个电子,B元素的原子失去1个电子后所形成微粒均与氩原子有相同的电子层结构。C元素的原子只有1个电子,D元素原子的M电子层数比N层电子数多6个。试写出:
(1)A、B、C、D的元素符号和名称:A____ B____C____D____。
(2)A元素的原子结构示意图____,D元素的离子结构示意图:______。
(3)画出A离子的电子式____B原子的电子式____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下图中甲池的总反应式为N2H4+O2===N2+2H2O。甲池中负极上的电极反应式为_________,乙池中石墨电极上发生的反应为_______________。甲池中每消耗0.1 mol N2H4,乙池电极上则会析出_________ g固体。

(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。下图为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。E为该燃料电池的_______极(填“正”或“负”)。F电极上的电极反应式为______________。

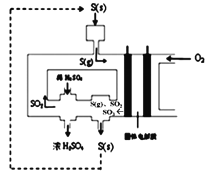
(3)下图为电化学法生产硫酸的工艺示意图,电池以固体金属氧化物作电解质,该电解质能传导O2-离子。S(g)在负极生成SO3的电极反应式为____________________。已知S(g)在负极发生的反应为可逆反应,为提高硫蒸气的转化率,该工艺采取的措施有____________(任写一条)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温、恒压下,在一个可变容积的容器中发生反应:A(g)+B(g) ![]() C(g)
C(g)
(1)若开始时放入1molA和1molB,达到平衡后,生成amolC,这时n(A)为________mol。
(2)若开始时放入3molA和3molB,达到平衡后,生成n(C)为________mol。
(3)若开始时放入x mol A、2mol B和1mol C,达到平衡后,A和C的物质的量分别是ymol和3amol,则x=________,y=________。平衡时,n(B)________(填序号)。
A.大于2mol B.等于2mol C.小于2mol D.可能大于、等于或小于2mol
(4)若在(3)的平衡混合物中再加入3molC,待再次到达平衡后,C的物质的量分数是________。
(5)若保持温度不变,在一个与(1)反应前起始体积相同、且容积固定的容器中发生上述反应。开始时放入1molA和1molB,达到平衡后,生成b molC,将b与a进行比较,则________(填序号)。
A.a<b B.a>b C.a=b D.不能比较
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应)。请回答下列问题:
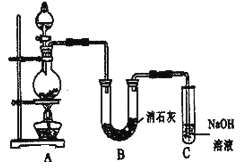
(1)A、B中的反应物分别是浓盐酸和MnO2。写出所发生的化学方程式__________,进入装置C的气体中所含杂质是_____、_____。
(2)漂白粉的有效成分是____(填化学式);D中所发生的化学反应的离子方程式是_______。
(3)此实验所得漂白粉的Ca(ClO)2产率偏低。该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应: ①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是__。②为避免另一副反应的发生,应采取的措施是________。
(4)若将该实验中残留的Cl2,缓慢通入KI溶液至过量,则溶液先变黄后变无色,且可检测到HIO3;写出并配平该“变无色”反应的化学方程式:________,若将KI改为KBr溶液,则溶液变为__色,未检测到HBrO3的存在。由上述事实推测,Cl2、HIO3、HBrO3的氧化性由强到弱的次序是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现代火法炼锌过程中发生了以下三个主要反应。下列说法正确的是
① 2ZnS(s) + 3O2(g)=2ZnO(s)+2SO2(g) △H1=a kJ mol-1
② 2C(s) +O2(g)=2CO(g) △H2=b kJ mol-1
③ ZnO(s) +CO(g)=Zn(g) +CO2(g) △H3=c kJ mol-1
A. 以上三个反应中,只有①是放热反应
B. 反应②的作用是仅为反应③提供还原剂
C. 用这种方法得到的是纯净的锌单质
D. 反应ZnS(s)+C(s)+2O2(g)=Zn(g)+SO2(g)+CO2(g)的△H=![]() kJ mol-1
kJ mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com