
【题目】无水MgBr2 可广泛用于有机反应催化剂、污水处理剂等。实验室可用镁屑与液溴为原料,采用下图装置制备无水MgBr2,请回答:
(1)识别下图中仪器。A的名称是______,B是_______
(2)实验时,可向装置C中缓慢通入干燥的氮气,直至溴完全导入三颈瓶中。干燥的氮气能将液溴吹出,因为液溴具有________的性质;实验中不能用干燥空气代替干燥N2,原因是:___________________________________________________________

(3)已知:Mg和Br2反应剧烈放热;乙醚(C2H5OC2H5)极易挥发。MgBr2和乙醚能发生如下反应:MgBr2+3C2H5OC2H5![]() MgBr2·3C2H5OC2H5+Q(Q>0);反应完毕后恢复至室温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0°C,析出晶体,再过滤得三乙醚合溴化镁粗品。第一次过滤除去的物质是_______。过滤必须用到的玻璃仪器是:_______。
MgBr2·3C2H5OC2H5+Q(Q>0);反应完毕后恢复至室温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0°C,析出晶体,再过滤得三乙醚合溴化镁粗品。第一次过滤除去的物质是_______。过滤必须用到的玻璃仪器是:_______。
(4)试用平衡移动的原理说明得到三乙醚合溴化镁后,加热有利于其分解,得无水MgBr2产品的原因: ______________________________
(5)为测定产品的纯度,可用EDTA(简写为Y4-)标准溶液滴定,反应的离子方程式:Mg2++Y4-====Mg Y2-
①滴定前润洗滴定管的操作方法是____________________________
②测定前,先称取0.2500g无水MgBr2产品,溶解后,用0.0500mol/L的EDTA 标准溶液滴定至终点,消耗EDTA 标准溶液26.50mL,则测得无水MgBr2产品的纯度是___________ (以质量分数表示)。
【答案】 干燥管 冷凝管 极易挥发 防止镁屑与氧气反应,生成副产物 MgO,且阻碍 Mg 和 Br2 的反应 镁屑 漏斗、烧杯、玻璃棒 加热促使乙醚挥发,且逆反应是吸热反应,加热后平衡朝有利于三乙醚合溴化镁分解的方向移动 从滴定管上口加入少量标准液,倾斜着转动滴定管,使液体润湿内壁,然后从下部放出,重复 2-3 次 97.5%
【解析】(1)根据图示,A是干燥管,B是冷凝管,故答案为:干燥管;冷凝管;
(2)干燥的氮气能将液溴吹出,因为液溴极易挥发,实验中不能用干燥空气代替干燥N2,因为镁能够与空气中的氧气反应生成氧化镁,阻碍 Mg 和 Br2 的反应,故答案为:极易挥发;防止镁屑与氧气反应,生成副产物 MgO,且阻碍 Mg 和 Br2 的反应;
(3)反应完毕后恢复至常温,过滤除去的固体为未反应的镁屑;冷却至0℃,析出晶体,过滤得三乙醚合溴化镁粗品;过滤必须用到的玻璃仪器有漏斗、烧杯、玻璃棒,故答案为:镁屑;漏斗、烧杯、玻璃棒;
(4)根据方程式MgBr2+3C2H5OC2H5![]() MgBr2·3C2H5OC2H5+Q(Q>0),加热促使乙醚挥发,且逆反应是吸热反应,加热后平衡朝有利于三乙醚合溴化镁分解的方向移动,故答案为:加热促使乙醚挥发,且逆反应是吸热反应,加热后平衡朝有利于三乙醚合溴化镁分解的方向移动;
MgBr2·3C2H5OC2H5+Q(Q>0),加热促使乙醚挥发,且逆反应是吸热反应,加热后平衡朝有利于三乙醚合溴化镁分解的方向移动,故答案为:加热促使乙醚挥发,且逆反应是吸热反应,加热后平衡朝有利于三乙醚合溴化镁分解的方向移动;
(5)①滴定前润洗滴定管是需要从滴定管上口加入少量待测液,倾斜着转动滴定管,使液体湿润内壁,然后从下步放出,重复2-3次,故答案为:从滴定管上口加入少量待测液,倾斜着转动滴定管,使液体润湿内壁,然后从下部放出,重复2-3次;
②依据方程式Mg2++Y4-═MgY2-分析,溴化镁的物质的量=0.0500mol/L×0.02650L=0.001325mol,则溴化镁的质量为0.001325mol×184g/mol=0.2438g,溴化镁的产品的纯度=![]() ×100%=97.5%,故答案为:97.5%。
×100%=97.5%,故答案为:97.5%。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】温度为T1℃时,在四个容积均为1L的恒容密闭容器中发生反应:2NO(g)+2H2(g)![]() N2(g)+2H2O(g) ΔH,该反应的速率表达式为v=k·cm(NO)·cn(H2)(k、m、n为常数),测得有关实验数据如下:
N2(g)+2H2O(g) ΔH,该反应的速率表达式为v=k·cm(NO)·cn(H2)(k、m、n为常数),测得有关实验数据如下:
容器编号 | 物质的起始浓度/(mol/L) | 速率/(mol·L-1·s-1) | 物质的平衡浓度/(mol/L) | |
c(NO) | c(H2) | c(N2) | ||
Ⅰ | 6×10-3 | 1×10-3 | a×10-3 | 2×10-4 |
Ⅱ | 6×10-3 | 2×10-3 | 2a×10-3 | |
Ⅲ | 1×10-3 | 6×10-3 | b×10-3 | |
Ⅳ | 2×10-3 | 6×10-3 | 4b×10-3 | |
下列说法正确的是( )
A. m=2,n=2
B. 达到平衡时,容器Ⅱ与容器Ⅳ的总压强之比为1:2
C. 温度升高为T2℃,测得平衡时,容器Ⅱ中c(H2O)=3.8×10-4mol/L,则ΔH>0
D. T1℃时,容器Ⅲ中达到平衡后再充入NO、H2O(g)各2×10-4mol,则反应将向逆反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒(34Se)与氧同主族,硒元素及其化合物与人体健康、工业生产密切相关。某科研小组以阳极泥(主要成分是Se,含有CuSe、Ag2Se等杂质)为原料,提炼硒的流程如下:

请回答下列问题:
(1)硒原子的次外层电子数_______,与硒同周期相邻元素是________(填元素名称)。
(2)已知A是Na2SeO3,可用于治疗克山病,则A的化学名称为______;C是Na2Se,则Na2Se的电子式为_______。
(3)上述流程图中的括号内“( )”,按操作先后顺序依次填写的内容是_____、_____。
(4)写出高温下用焦炭还原B的化学方程式___________________。
(5)溶液C中析出硒的离子方程式____________________。
(6)向Na2SeO3溶液中滴加稍过量的乙酸,其离子方程式为__________________。已知:Ka1(H2SeO3)=2.7×10-3、Ka2(H2SeO3)=2.5×10-8、Ka(CH3COOH)=1.8×10-5。
(7)粗硒可采用真空蒸馏的方法进行提纯,获得纯硒。真空蒸馏的挥发物中硒含量与温度的关系如图所示:

蒸馏操作中控制的最佳温度是________(填标号)。
A.455℃ B.462℃ C.475℃ D.515℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如图。下列对该实验的描述错误的是

A. 不能用水浴加热
B. 长玻璃管起冷凝回流作用
C. 为提纯乙酸丁酯,可用水和碳酸钠溶液洗涤
D. 通常加入过量1-丁醇以提高乙酸的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】开发、使用清洁能源发展“低碳经济”,正成为科学家研究的主要课题.氢气、甲醇是优质的清洁燃料,可制作燃料电池. 
(1)已知:①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H1=﹣1275.6kJmol﹣1②2CO(g)+O2(g)=2CO2(g)△H2=﹣566.0kJmol﹣1
③H2O(g)=H2O(l)△H3=﹣44.0kJmol﹣1写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(2)生产甲醇的原料CO和H2来源于:CH4(g)+H2O(g)CO(g)+3H2(g) ①一定条件下CH4的平衡转化率与温度、压强的关系如图a.则,P1P2;A、B、C三点处对应平衡常数(KA、KB、KC)的大小顺序为 . (填“<”、“>”“=”)
②100℃时,将1mol CH4和2mol H2O通入容积为1L 的反应室,反应达平衡的标志是: .
A.容器内气体密度恒定
B.单位时间内消耗0.1mol CH4同时生成0.3mol H2
C.容器的压强恒定
D.3v正(CH4)=v逆(H2)
③如果达到平衡时CH4的转化率为0.5,则100℃时该反应的平衡常数K=
(3)某实验小组利用CO(g)、O2(g)、KOH(aq)设计成如图b所示的电池装置,负极的电极反应式为 . 用该原电池做电源,常温下,用惰性电极电解200mL饱和食盐水(足量),消耗标准状况下的CO 224mL,则溶液的pH= (不考虑溶液体积的变化)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]﹣ , 铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍.因此,必须对含铬的废水进行处理,可采用以下两种方法. 【方法一】还原法 在酸性介质中用FeSO4等将+6价铬还原成+3价铬.具体流程如下:![]()
有关离子完全沉淀的pH如下表:
有关离子 | Fe2+ | Fe3+ | Cr3+ |
完全沉淀为对应氢氧化物的pH | 9.0 | 3.2 | 5.6 |
(1)写出Cr2O72﹣与FeSO4溶液在酸性条件下反应的离子方程式 .
(2)还原+6价铬还可选用以下的试剂(填序号).
A.明矾
B.铁屑
C.生石灰
D.亚硫酸氢钠
(3)在含铬废水中加入FeSO4 , 再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀.则在操作②中可用于调节溶液pH的试剂为:(填序号); A.Na2O2 B.Ba(OH)2 C.Ca(OH)2
此时调节溶液的pH范围在(填序号)最佳.
A.3~4 B.6~8 C.10~11 D.12~14
(4)【方法二】电解法 将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解.阳极区生成的Fe2+和Cr2O72一发生反应,生成的Fe3+和Cr3+在阴极区与OH一结合生成Fe(OH)3和Cr(OH)3沉淀除去. 写出阴极的电极反应式 .
(5)电解法中加入氯化钠的作用是: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)A和B反应生成C,假定反应刚开始只有A、B,它们的起始浓度均为1mol/L。反应进行2min后A的浓度为0.8mol/L,B的浓度为0.6mol/L,C的浓度为0.6mol/L。则在这2 min内反应的平均速率VA =_______ mol/(L· min),VB =________ mol/(L· min),该反应2 min内A、B、C三种物质的化学反应速率之比为:________________________。
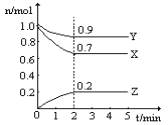
(2)某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如上图所示。根据图中数据,试填写下列空白:
①该反应的化学方程式为__________________________________________________;
②从开始至2min,Z的平均反应速率为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体内微量元素的含景其微,但是对人体的健康却起着重耍作用。下列各组元素全部是微量元素的是
A. Na、K、0、S B. Mo、Fe、Zn、Cu
C. N、H、0、P、C D. Fe、Ca、Cu、Mg、C
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com