
| A. | 该溶液中,K+、Cl-、HCOOH、I-可以大量共存 | |
| B. | 与Na2SO3反应的离子方程式:ClO-+SO32-═SO42-+Cl- | |
| C. | 不可使用pH试纸测定该溶液的pH | |
| D. | 1 L 0.1 mol/L该溶液和足量的CO2充分反应,产生10 g沉淀 |
分析 A.溶液中不能存在还原性离子;
B.发生氧化还原反应后,结合钙离子生成硫酸钙沉淀;
C.溶液具有漂白性;
D.和足量的CO2充分反应,生成碳酸氢钙和HClO.
解答 解:A.ClO-、I-发生氧化还原反应,不能大量共存,故A错误;
B.与Na2SO3反应的离子方程式为Ca2++ClO-+SO32-═CaSO4↓+Cl-,故B错误;
C.溶液具有漂白性,则不可使用pH试纸测定该溶液的pH,可选pH计测定,故C正确;
D.和足量的CO2充分反应,生成碳酸氢钙和HClO,则不能生成沉淀,故D错误;
故选C.
点评 本题考查物质的性质,综合性较强,涉及离子共存、氧化还原反应、与量有关的离子反应等,注重高频考点的考查,选项BD均为解答的易错点,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 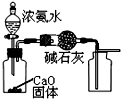 制取并收集干燥的NH3 | |
| B. | 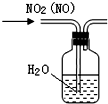 可除去NO2中的NO | |
| C. | 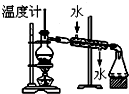 分离两种互溶但沸点相差较大的液体混合物 | |
| D. | 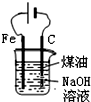 制备Fe(OH)2并能较长时间观察其颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
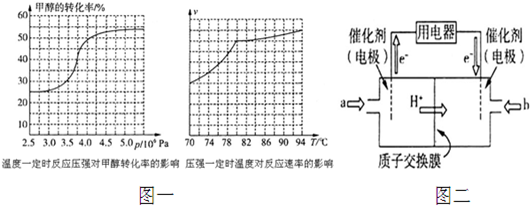
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | D元素处于元素周期表中第3周期第Ⅳ族 | |
| B. | 四种元素的原子半径:r(A)<r(B)<r(C)<r(D) | |
| C. | B、D的最高价氧化物中,B、D与氧原子均为双键 | |
| D. | 一定条件下,B单质能转换出D单质,C产单质能置换出A单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向氯化铝溶液中滴加过量氨水,生成白色胶状沉淀:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| B. | 加入足量的氢氧化镁以除去氯化镁溶液中的少量氯化铁:Fe3++3OH-═Fe(OH)3↓ | |
| C. | 常温下0.1mol/L 氯化铵溶液pH=5:NH4++H2O?NH3•H2O+H+ | |
| D. | 电解精炼铜时阳极铜溶解:Cu-2e-═Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应属加成反应 | B. | 乙烯可以通过石油裂解获得 | ||
| C. | 乙醇官能团为羟基 | D. | 乙醇、乙醛和乙酸互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
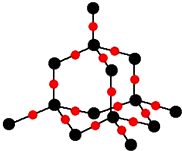 现代世界产量最高的金属是Fe、Al、Cu.
现代世界产量最高的金属是Fe、Al、Cu. )分子中碳原子杂化类型为SP2,分子中σ键比π键多5个.
)分子中碳原子杂化类型为SP2,分子中σ键比π键多5个.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
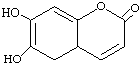
| A. | M的相对分子质量是178 | |
| B. | M有机物中含有2种官能团 | |
| C. | M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H9O5Na | |
| D. | 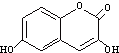 与M互为同分异构体 与M互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室里熔化氢氧化钠时,可选用石英坩埚和铁坩埚 | |
| B. | 不法商家制取的“地沟油”具有固定的熔沸点 | |
| C. | 食品保鲜膜按材质可分为聚乙烯(PE)、聚氯乙烯(PVC)、聚偏二氯乙烯(PVDC)等,PVC的单体可由PE的单体与氯化氢加成制得 | |
| D. | 家庭用食用醋代替CO2来增强漂白粉的漂白性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com