
| A. | 加热分解NH4Cl固体可以制得NH3 | |
| B. | Fe2O3是碱性氧化物,常用作红色油漆和涂料 | |
| C. | 硅单质常用来制作光导纤维和太阳能电池 | |
| D. | 浓硫酸具有脱水性,可以干燥Cl2 |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

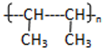 ,反应类型为加聚反应.
,反应类型为加聚反应.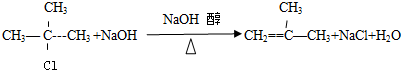 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
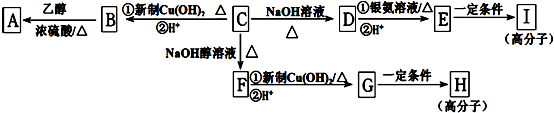
 ;
;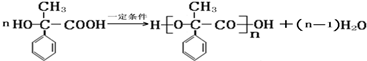 ,该反应类型是缩聚反应;
,该反应类型是缩聚反应; ,该反应类型是加聚反应;
,该反应类型是加聚反应; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性溶液中可能大量存在Fe2+、Cl?、NO3?、Na+ | |
| B. | 无色溶液中可能大量存在Mg2+、NH4+、Cl?、SO42- | |
| C. | 强碱性溶液中可能大量存在NH4+、K+、Cl?、SO42? | |
| D. | 酸性溶液中可能大量存在Fe3+、K+、I?、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
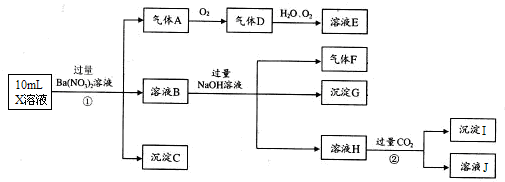
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用盐酸滴定氢氧化钠溶液时向锥形瓶中量取25.00mL的氢氧化钠溶液 | |
| B. | 用量筒测得排水法收集制得的氢气体积为50.28 mL | |
| C. | 用两只250 mL的容量瓶配制0.1 mol•L-1 500 mL的NaOH溶液 | |
| D. | 用托盘天平称取2.50 g胆矾,受热充分失水后,固体质量减轻0.90 g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
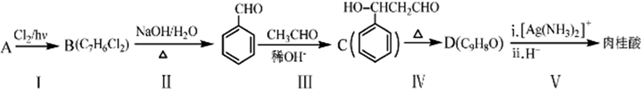
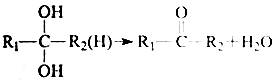

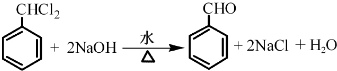 .
.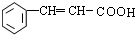 .肉桂酸的同分异构体中,符合下列条件的有3种,其中在1H核磁共振谱图中出现信号峰数量最少的异构体的结构简式是
.肉桂酸的同分异构体中,符合下列条件的有3种,其中在1H核磁共振谱图中出现信号峰数量最少的异构体的结构简式是 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com