
 在一定条件下,反应X(g)+3Y(g)?2Z(g)△H=-92.4 kJ/mol,X的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )
在一定条件下,反应X(g)+3Y(g)?2Z(g)△H=-92.4 kJ/mol,X的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )| A. | 图中A、B两点,达到相同的平衡体系 | |
| B. | 上述反应在达到平衡后,增大压强,H2的转化率提高 | |
| C. | 升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小 | |
| D. | 将1.0 mol X、3.0 mol Y,置于1 L密闭容器中发生反应,放出的热量为92.4 kJ |
分析 A、由图得出:A、B两点,X的平衡转化率(α)不同;
B、增大压强平衡向体积减小的方向移动;
C、升高温度正、逆反应速率都增大,逆反应速率比较正反应速率增大更多,平衡向逆反应方向移动;
D、可逆反应反应物不能完全转化,结合热化学方程式的含义解答.
解答 解:A、图中A、B两点,X的平衡转化率(α)不同,两者为不相同的平衡体系,故A错误;
B、增大压强平衡向体积减小的方向移动,即向正反应移动,X的转化率提高,故B正确;
C、升高温度正、逆反应速率都增大,逆反应速率比较正反应速率增大更多,平衡向逆反应方向移动,故C错误;
D、热化学方程式X(g)+3Y(g)?2Z(g)△H=-92.4kJ/mol表示1molX(g)和3molY(g)完全反应生成2molZ(g),放出的热量为92.4kJ,由于可逆反应反应物不能完全转化,1.0molX、3.0molY,置于1L密闭容器中发生反应,放出的热量小于92.4kJ,故D错误;
故选B.
点评 本题主要考查化学平衡图象、反应热计算、影响化学平衡与化学反应速率的因素等,难度中等,注意D中热化学方程式的意义.


科目:高中化学 来源: 题型:解答题
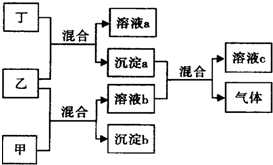 现有四瓶贴有甲、乙、丙、丁标签的溶液,它们可能是K2CO3、Ba(NO3)2、NaHSO4和K2SO4溶液.现进行如下实验,并记录部分现象(如图):
现有四瓶贴有甲、乙、丙、丁标签的溶液,它们可能是K2CO3、Ba(NO3)2、NaHSO4和K2SO4溶液.现进行如下实验,并记录部分现象(如图):查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ②⑤ | D. | ③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②④ | B. | 只有①② | C. | 只有①②③ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为56,中子数为30 |
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:多选题
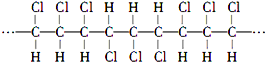 ;下列说法正确的是(双选)( )
;下列说法正确的是(双选)( )| A. | 聚合物的分子式是C3H3Cl3 | |
| B. | 聚合物的链节是 | |
| C. | 合成该聚合物的单体是CHCl═CHCl | |
| D. | 若n表示聚合度,则其相对分子质量为97n |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 电子由Pt电极流出,经外电路流向NiO电极 | |
| B. | Pt电极上发生的是还原反应 | |
| C. | NiO电极的电极反应式为NO+O2--2e-═NO2 | |
| D. | 每转移2 mol电子,有1 mol O2-迁移到负极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com