
����Ŀ���ҹ������������Ź�������ʱ�ھ���������������������� ˾ĸ�춦���Ⱦ�����ͭ������ͭ����Ҫ�ɷ���Cu����������������A���Sn��Pb���ش�����������
��1����̬Cuԭ�ӵļ۵����Ų�ͼ��___________________����̬Snԭ�ӵ�δ�ɶԵ�������Cu��__________����Pbλ�����ڱ���______________����
��2����CuSO4��Һ�м�������İ�ˮ�ټ������Ҵ�����������������ɫ������[Cu(NH3)4]SO4��H2O��
��SO42-��S���ӻ���ʽ��___________�����������ǽ����е縺����С��__________________��
�����ʾ��[Cu(NH3)4]2+�����е�ȫ����λ��____________��1mol[Cu(NH3)4]2+�к���_____mol������
��ˮ���ӵļ���Ϊ1050��С��NH3���Ӽ���1070�������˲����ԭ����_______________��
��3��ͭ����ģ����ͼ��ʾ��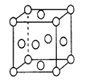 ��Cu�������ⳤΪbpm����1��ͭ������Cuԭ�ӵ�������____g��1��ͭ������Cuԭ��ռ�ݵ����Ϊ______________pm3��
��Cu�������ⳤΪbpm����1��ͭ������Cuԭ�ӵ�������____g��1��ͭ������Cuԭ��ռ�ݵ����Ϊ______________pm3��
���𰸡� ![]() 2 p sp3 H
2 p sp3 H 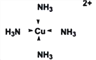 16 �µ��Ӷ�ռ�ݵĿռ�ϴ��ų�����ǿ�ڳɼ����Ӷ���ˮ�����д������Թµ��Ӷԣ���NH3�����д���1�Թµ��Ӷԣ���ˮ���Ӽ���С��NH3����
16 �µ��Ӷ�ռ�ݵĿռ�ϴ��ų�����ǿ�ڳɼ����Ӷ���ˮ�����д������Թµ��Ӷԣ���NH3�����д���1�Թµ��Ӷԣ���ˮ���Ӽ���С��NH3���� ![]() �� 4.25��10-22 ��
�� 4.25��10-22 ��
����������1����̬![]() ԭ����29��Ԫ�أ��۵����Ų�����
ԭ����29��Ԫ�أ��۵����Ų�����![]() ���ȫ���ĵ�����״̬���۵����Ų�Ϊ
���ȫ���ĵ�����״̬���۵����Ų�Ϊ![]() ����̬Snԭ�Ӻ�������Ų�1s2 2s2p6 3s23p63d10 4s24p64d10 5s25p2����̬Snԭ�ӵ�δ�ɶԵ�����Ϊ2��Cuԭ�ӵ�δ�ɶԵ�����Ϊ1�����߱�ֵΪ2��Pb���������Ų�Ϊ6s2 6p2������Pbλ�����ڱ���.P������ȷ����
����̬Snԭ�Ӻ�������Ų�1s2 2s2p6 3s23p63d10 4s24p64d10 5s25p2����̬Snԭ�ӵ�δ�ɶԵ�����Ϊ2��Cuԭ�ӵ�δ�ɶԵ�����Ϊ1�����߱�ֵΪ2��Pb���������Ų�Ϊ6s2 6p2������Pbλ�����ڱ���.P������ȷ����![]() ��2��P��
��2��P��
��2����![]() ��
��![]() ԭ�ӵ��ӻ���ʽΪ
ԭ�ӵ��ӻ���ʽΪ![]() ������ṹΪ����������
������ṹΪ����������![]() ���Ԫ��Ϊͭ�������⡢���������ķǽ�������ǿ��������������ǿ���縺����������Ԫ�أ���˵縺����С��Ϊ������ȷ�𰸣�sp3 ��H��
���Ԫ��Ϊͭ�������⡢���������ķǽ�������ǿ��������������ǿ���縺����������Ԫ�أ���˵縺����С��Ϊ������ȷ�𰸣�sp3 ��H��
��![]() �����еĻ�ѧ�������Ӽ������⼫�Լ���ͭ���ӺͰ�����λ��������[Cu(NH3)4]2+�����е�ȫ����λ��Ϊ
�����еĻ�ѧ�������Ӽ������⼫�Լ���ͭ���ӺͰ�����λ��������[Cu(NH3)4]2+�����е�ȫ����λ��Ϊ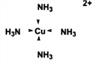 ��1mol[Cu(NH3)4]2+�к��е����3 mol����λ�� 1mol�����Ժ���4��4= 16mol��������ȷ�𰸣�
��1mol[Cu(NH3)4]2+�к��е����3 mol����λ�� 1mol�����Ժ���4��4= 16mol��������ȷ�𰸣� �� 16 ��
�� 16 ��
��ˮ���ӵļ���Ϊ1050��С��NH3���Ӽ���1070�������˲����ԭ���ǹµ��Ӷ�ռ�ݵĿռ�ϴ��ų�����ǿ�ڳɼ����Ӷԣ�ˮ�����д������Թµ��Ӷԣ���NH3�����д���1�Թµ��Ӷԣ���ˮ���Ӽ���С��NH3��������ȷ�����µ��Ӷ�ռ�ݵĿռ�ϴ��ų�����ǿ�ڳɼ����Ӷԣ�ˮ�����д������Թµ��Ӷԣ���NH3�����д���1�Թµ��Ӷԣ���ˮ���Ӽ���С��NH3���ӡ�
��3��ͭ����Ϊ������������������ͭԭ������Ϊ8��1/8+6��1/2=4,һ��������Cuԭ�ӵ�������4��64/NAg =![]() g��Cu�������ⳤΪbpm����Cuԭ�Ӱ뾶Ϊr=
g��Cu�������ⳤΪbpm����Cuԭ�Ӱ뾶Ϊr=![]() b/4pm, 1��ͭ������Cuԭ��ռ�ݵ����Ϊ4��4/3��r3=16/3��
b/4pm, 1��ͭ������Cuԭ��ռ�ݵ����Ϊ4��4/3��r3=16/3��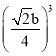 =��/12��
=��/12��![]() b)3 pm3����ȷ�𰸣�.
b)3 pm3����ȷ�𰸣�. ![]() �� 4.25��10-22 ����/12����
�� 4.25��10-22 ����/12����![]() b��3��
b��3��


 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����0.2molL��1�Ĵ����ˮϡ�ͣ���ͼ�е�����y��ʾ���ǣ������� 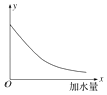
A.��Һ��OH�������ʵ���Ũ��
B.��Һ�ĵ�������
C.��Һ�е� ![]()
D.CH3COOH�ĵ���̶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ��������������Ȼ�������٣�ȴ��ά���������������ȱ�ٵġ��ù۵����ͨ��������һʵ���õ�֤������ ��
A. ȱMgʱҶƬ��� B. �Ͳ�ȱ��Cuʱ���֡�������ʵ��
C. ����ѪҺ���κ���̫�ͻ�鴤 D. ȱFe�����ƶѪ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����ñ�����ⶨNaOH��Һ��Ũ�ȣ��ü�����ָʾ�������в����п���ʹ�ⶨ���ƫ�͵��ǣ�������
A.��ʽ�ζ�����װ��Һǰδ�ñ�������Һ��ϴ2��3��
B.��ʼʵ��ʱ��ʽ�ζ��ܼ��첿�������ݣ��ڵζ�������������ʧ
C.��ƿ����Һ��ɫ�ɻ�ɫ���ɫ���������µζ�����Һ�����ڿ̶�
D.ʢNaOH��Һ����ƿ�ζ�ǰ��NaOH��Һ��ϴ2��3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������д�������ƽ�⣺CO��g��+H2O��g��CO2��g��+H2��g����CO2��g����ƽ�����ʵ���Ũ��c��CO2�����¶�T�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ������� 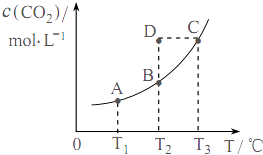
A.ƽ��״̬A��C��ȣ�ƽ��״̬A��c��CO��С
B.��T2ʱ������Ӧ����״̬D����һ����V����V��
C.��ӦCO��g��+H2O��g��CO2��g��+H2��g���ġ�H��0
D.��T1��T2ʱ��ƽ�ⳣ���ֱ�ΪK1��K2 �� ��K1��K2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���淴Ӧ�ڲ�ͬ��Ӧʱ������ʵ����ʵ����ı仯�������ͼ��ʾ��
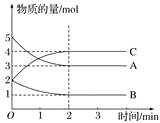
�ش��������⣺
(1)�÷�Ӧ�ķ�Ӧ����________����������________����ѧ����ʽΪ_____________________��
(2)��Ӧ��ʼ��2 minʱ���ܷ���C��Ũ�ȱ仯�����㷴Ӧ���ʣ�Ϊʲô��________________________________________________________________________��
(3)2 min��A��B��C�����ʵ���������ʱ��ı仯���仯��˵������������£���Ӧ�Ѵﵽ��______________״̬��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
A. ����C��H��O��N��S��P��Ԫ��
B. ��ֻ����һ��������һ���Ȼ�
C. �����Ȼ��������백����ˮ����
D. ����˳��ͬ�ǵ����ʶ����Ե�ԭ��֮һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijԪ������������Ӧ��ˮ����ķ���ʽ��H4RO4��������̬�⻯��ķ���ʽ�ǣ� ��
A.RH3B.RH4C.H2RD.HR
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(Y)������Ҫ�Ĺ�����ֵ��������ȿ����ѱ��ٿݽߡ�ͨ������������ʯ���Եõ�Y3+�Ľ���Һ��
��1 ����Һ�ɷ�
Al3+ | Fe3+ | Ca2+ | PO43- | Mg2+ | Mn2+ | Y3+ | |
Ũ��/(mgL-1) | 7670 | 9460 | 550 | 640 | 5600 | 1500 | 70.2 |
��1������Һ�����л��ܼ���HR��������ȡ��ʵ��Y3+�ĸ�������֪��Y3+��Fe3+�������ƣ���ԭ�����£�Fe3+ + 3HR ![]() FeR3 + 3H+ Y3+ + 3HR
FeR3 + 3H+ Y3+ + 3HR ![]() YR3 + 3H+ ����֪��FeR3��YR3��������HR��
YR3 + 3H+ ����֪��FeR3��YR3��������HR��
����Һ�ڲ�ͬpH����ȡ�Ľ����ͼ1��

���û�ѧƽ��ԭ�����ͣ���pH����Y3+��ȡ�������ԭ��________��
�ڽ��ͼ1���ͣ���ҵ����ȡY3+֮ǰ��Ӧ���ȳ�ȥFe3+��ԭ����________��
��2���������кͳ��������������ᷨ�����Գ�����
��2 Fe3+��Y3+ȥ����
�յ�pH | ȥ����/% | |
Fe3+ | Y3+ | |
3.0 | 87.84 | 19.86 |
3.5 | 92.33 | 23.63 |
4.5 | 99.99 | 44.52 |
5.0 | 99.99 | 89.04 |
�кͳ������������Һ�м���NaOH��Fe3+��ȥ�������2��ʾ��
�ٸ�ʵ�������£�Fe3+ȥ���ʱ�Y3+��Ŀ���ԭ��________��
���ᷨ�������ᣨH3PO4����Ԫ���ᣩ���뵽����Һ�У��ټ���Na2CO3��Һ����pHΪ2.5�����˳�ȥ������������FePO4������Һ��ʣ���Fe3+��Y3+Ũ�����3��
��3 ��Һ��Fe3+��Y3+��Ũ��
Fe3+ | Y3+ | |
Ũ��/(mgL-1) | 508 | 68.9 |
�� ��ƽ�����ᷨ�����������е����ӷ���ʽ
Fe3+ + + = FePO4��+ CO2��+ ��___________________
�� �ۺϷ�����1����2����3����ҵ�ϲ��������ᷨ��������ԭ��________��
��3���������ᷨ�����������л��ܼ�HR��ȡY3+����ͨ��________����������ռ���Y3+���л���Һ��
��4���ۺϷ������ϲ��ϣ�����˵����������________��
a. ����ͼ1��֪��pH��0.2��2.0��Χ�ڣ��л��ܼ��е�Fe3+����ˮ��Һ�е�Fe3+
b. ��2�� Y3+��ʧ����20%���ҵ�ԭ����������ɵ�Fe(OH)3��Y3+������
c. ��2�� pH��4.5��5.0��Χ�ڣ�Y3+��ʧ�ʱ��Ŀ���ԭ��Y3+ + 3OH- = Y��OH��3��
d. �л��ܼ���ȡY3+���ŵ���Ca2+��Mg2+��Mn2+�Ƚ���������ȡ�ʼ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com