
| A. | 金属性:Na<Mg<Al | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 酸性强弱:H4SiO4<H3PO4<HClO4 | D. | 原子半径大小:Na>S>Cl |
分析 A.同一周期中,原子序数越大金属性越弱;
B.非金属性越强,对应简单氢化物的稳定性越强;
C.非金属性越强,最高价氧化物对应水合物的酸性越强;
D.同一周期中,原子序数越大,原子半径越小.
解答 解:A.Na、Mg、Al位于同一周期,原子序数越大金属性越弱,则金属性:Na>Mg>Al,故A错误;
B.非金属性Cl>S>P,对应简单氢化物的热稳定性:HCl>H2S>PH3,故B正确;
C.非金属性:Si<P<Cl,最高价含氧酸的酸性:H4SiO4<H3PO4<HClO4,故C正确;
D.原子半径大小:Na>S>Cl,故D正确;
故选A.
点评 本题考查原子结构与元素周期律的关系,题目难度不大,明确元素周期律的内容即可解答,注意掌握原子结构与元素周期律、元素周期表的关系,试题有利于提高学生的综合应用能力.


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸与氧化亚铁反应 | B. | 浓硫酸与木炭粉反应 | ||
| C. | 浓硫酸与氧化铜反应 | D. | 浓硫酸与氯化钠固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | z=2 | |
| B. | 2 s 后,容器内的压强是初始的 $\frac{7}{8}$ 倍 | |
| C. | 2 s 后,B 的浓度为 0.5 mol/L | |
| D. | 2 s 时 C 的体积分数为 $\frac{2}{7}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
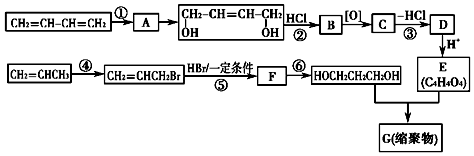
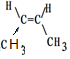 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用丁达尔效应是区分胶体与溶液的一种常用物理方法 | |
| B. | 在煮沸的氢氧化钠溶液中滴加5~6滴饱和氯化铁溶液可制得氢氧化铁胶体 | |
| C. | 利用的胶体聚沉的性质在豆浆里加入盐卤做豆腐 | |
| D. | 胶体区别于其它分散系的本质特征是分散至粒子直径的大小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷分子中C、H间是非极性键 | B. | 甲烷分子是空间三角锥结构 | ||
| C. | 甲烷的结构式为CH4 | D. | 沼气、天然气的主要成份都是甲烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 42He原子核内含有4个质子 | |
| B. | 32He和42He互为同位素 | |
| C. | 32He原子核内含有3个中子 | |
| D. | 42He的最外层电子数为2,所以具有较强的金属性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表中有7个横行即7个周期,有18个纵行,共16个族 | |
| B. | 在周期表的右上角可找到耐高温、耐腐蚀的材料 | |
| C. | 因为等浓度的HI和HCl的酸性:HI>HCl,所以非金属性:I>Cl | |
| D. | 在周期表中与IIA相邻的是IA和IIIA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com