
����Ŀ����1������Ӫ��ƽ�⣬�DZ�֤���Ľ��������������������Ч�ֶΡ�
�١��й�����ƽ����ʳ������������ͼ����λ�ڵڡ��ݡ�����ÿ�첻����25g������������________������ĸ����
a.���� b.��֬ c.����
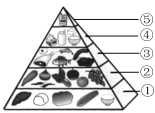
���ҹ�������ƽʱ����ʳ��Ӧ��Լ���ʳ�����ʳ�����ڼ���ʳ�����________������ĸ����
a.����� b.���� c.ƻ��
����ɫֲ��ͨ����ͼ�����������û�ѧ����ʽ��ʾ�������õĹ��̣�____________________��

��2����������������ͷ�չ�����ʻ���������ʹ�ò��Ͽ��Ը����������
���ҹ������г����켼��������������ˮƽ�������г�����Ҫʹ�����ʽ������ϡ����п�����Ϊ���ʽ������ϵ���________������ĸ����
a.���Ͻ� b.���Ͻ� c.̼��ά d.����ά
����ͭ���ҹ����ƾõ���ʷ����ͭ����Ҫ���Ԫ����ͭ��________����Ԫ�ط��ţ�����ͭ��������������һ�㱡����ͭ��[��Ҫ�ɷ���Cu2(OH)2CO3]����д��ͭ�ڳ�ʪ�Ŀ����з����绯ѧ��ʴʱ��������Ӧʽ��_________________________________________��
�������л��������Ժã����ᣬ���ᡢ����ڼӹ����ͣ�ǿ�ȸߣ���ȫ�Ժá��л���������________����ϳ���ά�����ϳ��������ϡ������ϡ��ط��������ķ���ϩ������Ϊ��ճ��Ϳ�㣬д���þۺ���Ľṹ��ʽ��_____________________________��
��3�����ֽྻ��ȫ�����滷���ѳ�Ϊȫ����Ĺ�ʶ��������ȻҪ��г�ദ��
��úֱ̿��ȼ��������ֻ������⡣������������ʴ�����������������Լ���������________������ĸ����
a.Ca(OH)2 b.KNO3 c.SiO2 d.CaCO3
�ڴ�����CO��SO2�̵�����Ⱦ��һ�ַ����ǽ�CO��SO2�ڴ���������ת��Ϊ������д��������Ӧ�Ļ�ѧ����ʽ��_____________________________��
�۾�����������֯������ȫ����75%���ҵļ�����ˮ����Ⱦ�йء���ˮ���������ܶ࣬���纬��(CN-)��ˮ�Ĵ��������ڼ��������£������ˮ��ͨ��Cl2���ɽ�CN-����Ϊ����N2��CO2��ʹˮ�ʵõ�������д���÷�Ӧ�����ӷ���ʽ��_____________________________��
������������ˮ����������Ҫ�Ļ���֮һ����������չ����ClO2��O3���������Һ�ȣ���Ҫ�����Ƿ���Һ��������ʹˮ�еĶ����л�����仯�������к���������___________�������ʽ���������°����»���
���𰸡� b bc nCO2+mH2O![]() Cn(H2O)m+nO2 a Sn O2+2H2O+4e-==4OH- ����
Cn(H2O)m+nO2 a Sn O2+2H2O+4e-==4OH- ���� ![]() ad 2CO+SO2
ad 2CO+SO2 ![]() S+2CO2 2CN-+5Cl2+8OH-==N2+2CO2+10Cl-+4H2O CHCl3
S+2CO2 2CN-+5Cl2+8OH-==N2+2CO2+10Cl-+4H2O CHCl3
����������1����λ�ڵڡ�5���㼴���㣬��ÿ�첻����25g��������������֬����ѡb�����������Ҫ�������ʣ���������ʳ��߲ˡ�ˮ�����ڼ���ʳ���ѡbc���۱�ʾ�������ù��̵ķ���ʽΪnCO2+mH2O![]() Cn(H2O)m+nO2����2����a�����ܶ�С�����Ͻ�Ϊ��������ϣ���ʴ��Ӳ�ȴ��ϸ����г�����ʹ�ò���Ҫ��a��ȷ��b�����Ͻ�����������ϣ�b����c��̼��άΪ�ǽ������ϣ������ϸ����г�����ʹ�ò���Ҫ��c����d������άΪ�ǽ������ϣ������ϸ����г�����ʹ�ò���Ҫ��d����ѡa������ͭ����Ҫ���Ԫ����ͭ��Sn��ͭ�ڳ�ʪ�Ŀ����з����绯ѧ��ʴʱ���������õ����ӣ�������ӦʽΪO2+2H2O+4e-��4OH-�����л������������ϲ��ϡ��ط��������ķ���ϩ������Ϊ��ճ��Ϳ�㣬�þۺ���ĵ������ķ���ϩ���߾���Ľṹ��ʽΪ
Cn(H2O)m+nO2����2����a�����ܶ�С�����Ͻ�Ϊ��������ϣ���ʴ��Ӳ�ȴ��ϸ����г�����ʹ�ò���Ҫ��a��ȷ��b�����Ͻ�����������ϣ�b����c��̼��άΪ�ǽ������ϣ������ϸ����г�����ʹ�ò���Ҫ��c����d������άΪ�ǽ������ϣ������ϸ����г�����ʹ�ò���Ҫ��d����ѡa������ͭ����Ҫ���Ԫ����ͭ��Sn��ͭ�ڳ�ʪ�Ŀ����з����绯ѧ��ʴʱ���������õ����ӣ�������ӦʽΪO2+2H2O+4e-��4OH-�����л������������ϲ��ϡ��ط��������ķ���ϩ������Ϊ��ճ��Ϳ�㣬�þۺ���ĵ������ķ���ϩ���߾���Ľṹ��ʽΪ![]() ����3����������������ʴ�����������������Լ�����������ʯ�һ�̼����к��ᣬ��ѡad���ڴ�����CO��SO2�̵�����Ⱦ��һ�ַ����ǽ�CO��SO2�ڴ���������ת��Ϊ����������Ӧ�Ļ�ѧ����ʽΪ2CO+SO2
����3����������������ʴ�����������������Լ�����������ʯ�һ�̼����к��ᣬ��ѡad���ڴ�����CO��SO2�̵�����Ⱦ��һ�ַ����ǽ�CO��SO2�ڴ���������ת��Ϊ����������Ӧ�Ļ�ѧ����ʽΪ2CO+SO2![]() S+2CO2���ۺ���(CN-)��ˮ�Ĵ��������ڼ��������£������ˮ��ͨ��Cl2���ɽ�CN-����Ϊ����N2��CO2�����ݵ��ӵ�ʧ�غ㡢ԭ���غ�͵���غ��֪�÷�Ӧ�����ӷ���ʽΪ2CN-+5Cl2+8OH-��N2+2CO2+10Cl-+4H2O��������ClO2��O3���������Һ�ȣ���Ҫ��Һ��������ʹˮ�еĶ����л�����仯�������к���������CHCl3�������°����»���
S+2CO2���ۺ���(CN-)��ˮ�Ĵ��������ڼ��������£������ˮ��ͨ��Cl2���ɽ�CN-����Ϊ����N2��CO2�����ݵ��ӵ�ʧ�غ㡢ԭ���غ�͵���غ��֪�÷�Ӧ�����ӷ���ʽΪ2CN-+5Cl2+8OH-��N2+2CO2+10Cl-+4H2O��������ClO2��O3���������Һ�ȣ���Ҫ��Һ��������ʹˮ�еĶ����л�����仯�������к���������CHCl3�������°����»���


 �¿α�����Ķ�ѵ��ϵ�д�
�¿α�����Ķ�ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں����ܱ�������ͨ��X��������Ӧ��2X(g)![]() Y(g)���¶�T1��T2��X�����ʵ���Ũ��c(x)��ʱ��t�仯��������ͼ��ʾ������������ȷ���ǣ� ��
Y(g)���¶�T1��T2��X�����ʵ���Ũ��c(x)��ʱ��t�仯��������ͼ��ʾ������������ȷ���ǣ� ��
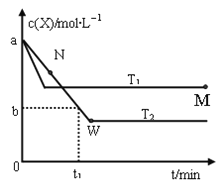
A. �÷�Ӧ���е�M��ų����������ڽ��е�W��ų�������
B. T2�£���0��t1ʱ���ڣ���(Y)��![]() mol/(L��min)
mol/(L��min)
C. M�������Ӧ���ʦ�������N����淴Ӧ���ʦ���
D. M��ʱ�ټ���һ������X��ƽ���X��ת��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ��ش��������⣺
��1���� 28.5 g �Ȼ�þ����ˮ��ɵ� 500mL ��Һ�� Cl-Ũ����______________��д���Ȼ�þ�ĵ��뷽��ʽ_________________________________________________________��
��2���������� 50 g �� HCl��NH3��CO2��O2 �������壬����ͬ�¶Ⱥ���ͬѹǿ�����£����������____________��
��3������ 90 mL 0.1 mol/L CuSO4 ��Һ����Ҫ CuSO4��5H2O_______ g�����в�����ʹ������ҺŨ��ƫ�ߵ���__________________________��
A.����ƿϴ�Ӹɾ���δ���� B.���ݺ���ҡ�ȡ����ã�����Һ���½����ټ�����������ˮ
C.����ʱ���ӿ̶��� D.�ձ��Ͳ�����δϴ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼Ԫ�������ǵ��ճ��������Ϳ�ѧ�о��ܲ��ɷ֡���ش��������⡣
(1)��ϩ����ˮ������Ĺ�Ч,��ϩ�ĵ���ʽ��______________��
(2)Al2O3���̼�Ȼ�ԭһ�Ȼ�����һ���µ���������,�÷����̶�,�豸��,����Ŀǰ�����ᳫ���ܼ��š����������Ĵ���
������ұ�������з����ķ�Ӧ�У�
(��)2Al2O3(s)+9C(s)=Al4C3(s)+6CO(g) ��H1;
(��)Al2O3(s)+Al4C3(s)+3AlCl3(g)=9AlCl(g)+3CO(g) ��H2;
(��)3AlCl(g)=AlCl3(g)+2Al(l) ��H3;
��Al2O3(s)+3C(s)= 2Al(l)+ 3CO(g) ��H4=___________________(�ú���H1����H2����H3�Ĵ���ʽ��ʾ)��
��Al4C3�����̼�Ȼ�ԭһ�Ȼ����������м�����������ˮ��Ӧ��������л���÷�Ӧ�Ļ�ѧ����ʽΪ__________________________________��
(3)���û���̿�Ļ�ԭ�Կɴ�����������β��(��������),�������·�ӦC(s)+2NO(g)![]() N2(g)+CO2(g) ��H��0��һ��������,�ܱ������е��й����ʵ�Ũ����ʱ��ı仯���±���ʾ��
N2(g)+CO2(g) ��H��0��һ��������,�ܱ������е��й����ʵ�Ũ����ʱ��ı仯���±���ʾ��
ʱ��/mim Ũ��/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 2.0 | 1.16 | 0.40 | 0.40 | 0.6 | 0.6 |
N2 | 0 | 0.42 | a | b | 1.2 | 1.2 |
CO2 | 0 | 0.42 | a | b | 1.2 | 1.2 |
��0~20min�ڵ�ƽ����Ӧ����v(CO2)=_______mol��L-1��min-1����һ�δﵽƽ���ƽ�ⳣ��K=__________��
��30minʱֻ�ı�ijһ��������ı������������______________ (����ĸ���)��
a�������¶� b�������¶� c����ͨ��һ������NO
d����С��������� e��������ʵĴ��� f�����������ݻ�
(4)����¯�з������ӵĻ�ѧ��Ӧ,���а�����Ӧ��C(s)+CO2(g)![]() 2CO(g)��H>0����1molCO2��������̼���뵽һ����ѹ�ܱ������У���ѹǿΪP�����ﵽƽ��ʱ,��������������������¶ȵĹ�ϵ����ͼ��
2CO(g)��H>0����1molCO2��������̼���뵽һ����ѹ�ܱ������У���ѹǿΪP�����ﵽƽ��ʱ,��������������������¶ȵĹ�ϵ����ͼ��

��CO2�������Ϊ86%ʱ,CO2��ת����Ϊ______________%(�������һλС��,��ͬ)��
����֪�������ѹP��=P������������������ﵽƽ��ʱ������ķ�ѹ��������Ũ������ʾ��ƽ�ⳣ��ΪKp,��900��ʱ,Kp=______________(�ú�p���Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���������ڿ������ܱ����������������ơ�ij��ȤС��Ϊ�����������ƹ����Ƿ���ʼ�̽��������������ʣ����������ʵ��:

I������Na2SO3�Ƿ����
��1����Բ����ƿA�м������Һ1.0 mol/LNa2SO3��Һ50mL��ҺaΪ_______����ҺbΪ_______��
��2����װ��A�еμ�������Һa��Na2SO3��Ӧ��ȫ����װ��AʹSO2��ȫ�ݳ���ʵ��ǰ����Cװ������2.4g����Na2SO3��Һ���ʵ���Ũ��Ϊ_______mol/L�����ж�Na2SO3�����Ƿ����______�����ǻ����

II����������װ���Ʊ�����SO2�����ʵ��Ƚ�H2SO3�� H2CO3��H2SiO3������ǿ������̽��SO2�Ļ�ѧ���ʡ�
��1���Լ�X��___________���Լ�Y��___________���Լ�Z��___________��
��2���ر�ֹˮ��b����ֹˮ��a����װ����ͨ��SO2�����۲쵽_________����֤��H2CO3���Ա�H2SiO3ǿ��
��3���ر�ֹˮ��a����ֹˮ��b������ͨ��SO2����ˮ��ɫ��˵��SO2����_______��д����Ӧ�����ӷ���ʽ______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��̽������֤���������ʣ�ij�о���ѧϰС����MnO2��Ũ����Ϊ��Ҫԭ�ϣ��������ͼ��ʾװ��(����a������ע������ͷ����Ƥ�ܣ���ͷ�Ѳ��벢������Ƥ��)�������о���
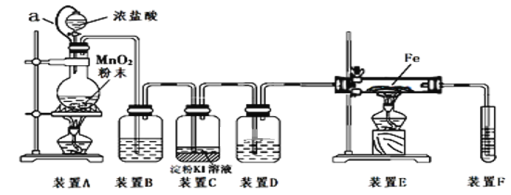
�����ϣ�����������Ӧ��ȡ�Ȼ���Ҫ����ˮ�����½��У�
�Իش��������⣺
��l��װ��A�з�����Ӧ�Ļ�ѧ����ʽΪ_____________________��
��2��װ��B�е��Լ�Ϊ_________��װ��D������________��
��3��װ��C�з�����Ӧ�����ӷ���ʽΪ_____________________________��
��4����Ӧ��ʼ��װ��E������Ӧ�Ļ�ѧ����ʽΪ____________________________��
��5��װ��F�з�����Ӧ�Ļ�ѧ����ʽΪ________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������(FeC2O4�� 2H2O)��һ�ֻ�ɫ������ˮ�Ĺ��壬�����ֽ⣬������﮵�ء�Ϳ�ϡ���ɫ���Լ��й���ϵ�ԭ���ϡ�
I���Ʊ������������壺
�� ��ȡ��������茶���5 g������250 mL������ƿ�У�����10������1.0 mol��L-1 H2SO4��Һ��15 mL����ˮ�����ܽ⣻
�� ����25 mL���Ͳ�����Һ�����Ƚ������У�ֹͣ���ȣ����ã�
�� ����ɫ����FeC2O42H2O������������ϴ�ӣ�����Լ20 mL����ˮ���貢����5 min�����ã���ȥ�ϲ���Һ�����û�ɫ�����������塣

�ش��������⣺
��1������C��������_____________������B��������_____________
��2�� ��������茶����������ܽ��ԭ����_____________________
��3����������茶�����ܻ���һ��Fe3+���ǰ�(NH2OH��������������NH3OH+��ʽ����)����ǿ��ԭ�ԣ������ǰ�ȥ���������е�Fe3+��д����ص����ӷ���ʽ___________________________________
II��̽�����������Ĵ��ȣ�
�� ȷ��ȡm g��������������Ʒ(���в��������)������25 mL 2 mol��L-1H2SO4��Һ�У���60~80��ˮԡ���ȣ���100 mL����ƿ���100.00 mL��Һ��
�� ȡ������Һ20.00 mL����KMnO4����Һ(Ũ��Ϊc mol��L-1)�ζ����Σ�ƽ������V1 mL��
�� ��������п�ۺ�2 mL 2 mol��L-1 H2SO4��Һ����Ӧһ��ʱ���ȡ1����Һ���ڵ�ΰ��ϼ��飬��Fe3+������
�� ���˳�ȥп�ۣ���Һ�ռ�����һ����ƿ�У�����ֽ����������ϴ�ӣ�ϴ��Һ������Һ�У��ٲ���Լ2~3 mL 2 mol��L-1 H2SO4��Һ��������KMnO4����Һ(Ũ��Ϊc mol��L-1)�ζ����յ㣬��ƽ�вⶨ���Σ�ƽ������V2 mL��
�ش��������⣺
��4���ڢ�����Һ�з���MnO4��+8H++5Fe2+==5Fe3++Mn2++4H2O��������һ������ԭ��Ӧ��д�������ӷ���ʽ_____________________________________����KMnO4����Һ�ζ����յ��������________________________________________
��5����������п�۵�Ŀ����______________________________________��������м�����������Fe3+���Լ�������______________��Һ
��6������m g������Ʒ�Ĵ���Ϊ______________(�ú�c��V1��V2��ʽ�ӱ�ʾ�����ػ���)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1������ʽΪC8H18��һ�ȴ���ֻ��һ�ֵ�����������Ϊ________________��
��2�������Ľṹ��ͼ��ʾ�������ʽΪ___________����һ�ȴ�����_____�֣����ȴ�����_____�֡�
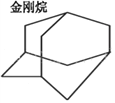
��3�������ϩ(CH2=C(CH3)CH=CH2)��˳ʽ�������ϩ�Ľṹ��ʽΪ_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij��ѧ��Ӧ��ƽ�ⳣ������ʽΪK��![]() ���ڲ�ͬ���¶��¸÷�Ӧ��
���ڲ�ͬ���¶��¸÷�Ӧ��
ƽ�ⳣ�������ʾ
t �� | 700 | 800 | 830 | 1000 | 1200 |
K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
�����й�������ȷ���ǣ� ��
A. �÷�Ӧ�Ļ�ѧ����ʽ�ǣ� H2(g)��CO2(g) ![]() CO(g)��H2O(g)
CO(g)��H2O(g)
B. ������Ӧ������Ӧ�����ȷ�Ӧ
C. �����һ��������ܱ������м���CO2��H2��1 mol��5 min���¶����ߵ�830 �棬�����ʱ���CO2Ϊ0.5 mol����÷�Ӧ�ﵽƽ��״̬
D. ij�¶��£����ƽ�ⳣ���������й�ϵʽ�� ![]() ��
��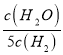 �����ʱ�¶�700��
�����ʱ�¶�700��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com