
有NaCl、FeCl2、FeCl3、MgCl2、AlCl3五种溶液,用一种试剂就可把它们鉴别开来,这种试剂是
A.盐酸 B.氨水 C.烧碱溶液 D.KSCN溶液
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源:2013-2014江苏省第二学期期中考试高一化学试卷(解析版) 题型:选择题
对于反应2SO2+O2 2SO3下列判断正确的是
2SO3下列判断正确的是
A.2 mol SO2和足量的O2反应,必生成2 mol SO3
B.平衡时SO2、O2、SO3的分子数之比为2∶1∶2
C.平衡时SO2的消耗速率必定等于O2的生成速率的2倍
D.平衡时SO2的浓度必为O2浓度的2倍
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省淮安市高三5月信息卷化学试卷(解析版) 题型:选择题
常温下,下列各溶液的叙述中正确的是
A.NaHSO3与Na2SO3混合溶液中:3c(Na+) = c(HSO3-) + c(SO32-)
B.0.1mol·L-1的醋酸钠溶液20 mL与0.1mol·L-1盐酸10 mL混合后溶液显酸性
c (CH3COO-)>c (Cl-)>c (CH3COOH)>c (H+)
C.等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:
c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-)
D.向1.00 L 0.3mol·L-1NaOH溶液中缓慢通入0.2molCO2气体,溶液中:
c(Na+) > c(CO32-) > c(HCO3-) > c(OH-) > c(H+)
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省海门市第一学期期末教学质量调研高一化学试卷(解析版) 题型:实验题
(10分)化学小组同学依据化学反应Zn+2H2SO4(浓) ZnSO4+SO2↑+2H2O制取22.4 L(标准状况)SO2气体。取65.0 g锌粒与98%的浓H2SO4(ρ=1.84 g·cm-3)110 mL充分反应,锌全部溶解。对于制得的气体,有同学认为可能混有氢气。为此,化学小组的同学设计了如下实验装置,对所制取的气体进行探究。
ZnSO4+SO2↑+2H2O制取22.4 L(标准状况)SO2气体。取65.0 g锌粒与98%的浓H2SO4(ρ=1.84 g·cm-3)110 mL充分反应,锌全部溶解。对于制得的气体,有同学认为可能混有氢气。为此,化学小组的同学设计了如下实验装置,对所制取的气体进行探究。

请回答下列问题:
(1)装置A中添加液体的仪器名称为 ;98%的浓H2SO4(ρ=1.84 g/cm3)的物质的量浓度是 ;
(2)请写出产生氢气的反应的离子方程式 ;
(3)①装置B是为了吸收SO2,则不能选用下列试剂中的 (填序号);
A.NaOH溶液 B.浓H2SO4 C.KMnO4溶液
②可证实一定量的锌粒和一定量的浓硫酸反应后生成的气体中混有氢气的实验现象是 ;
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省海门市第一学期期末教学质量调研高一化学试卷(解析版) 题型:选择题
下列各组物质不能实现直接转化的是
A.S→SO2→H2SO4→MgSO4 B.Cu→CuCl2→Cu(NO3)2→Cu(OH)2
C.Al→Al2O3→Al(OH)3→NaAlO2 D.Na→Na2O→Na2CO3→NaCl
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省海门市第一学期期末教学质量调研高一化学试卷(解析版) 题型:选择题
环境污染已成为人类社会面临的重大威胁,下列对应关系不正确的是
| 环境问题 | 造成环境问题的主要物质 |
A | 酸雨 | 二氧化硫 |
B | 温室效应 | 二氧化碳 |
C | 白色污染 | 二氧化硅 |
D | 光化学烟雾 | 二氧化氮 |
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省泰州市姜堰区高二下学期期中考试 化学试卷(解析版) 题型:选择题
下列有关同分异构体数目的叙述中,错误的是
A.甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种
B.含有5个碳原子的饱和链烃,其一氯取代物共有8种
C.与 互为同分异构体的芳香族化合物有6种
互为同分异构体的芳香族化合物有6种
D.菲的结构简式为 ,可有5种一硝基取代物
,可有5种一硝基取代物
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省无锡市高一下学期期末考试化学试卷(解析版) 题型:填空题
乙酸乙酯可以做白酒勾兑用香料、人造香精。实验室制乙酸乙酯的主要装置如图7所示,主要步骤:①在a试管中按3∶2∶2的体积比配制浓硫酸、乙醇、乙酸的混合物;②按图7连接装置,使产生的蒸气经导管通到b试管所盛的饱和碳酸钠溶液中;③小火加热a试管中的混合液;④等b试管中收集到约2 mL产物时停止加热。撤下b试管并用力振荡,然后静置待其中液体分层;⑤分离出乙酸乙酯。(加热装置略)
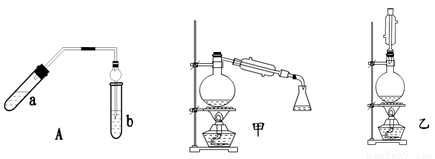
图7 图8 图9
请回答下列问题:
(1)步骤①中,配制混合溶液的正确操作是 。
(2)步骤②中b试管中饱和Na2CO3溶液的主要作用 。(填字母)
a. 降低乙酸乙酯的溶解度
b. 除去实验中挥发出来的硫酸
c. 除去乙酸乙酯中混有的乙酸和乙醇
(3)图7装置中使用球形干燥管除起到冷凝作用外,另一重要作用是 ,步骤⑤中分离乙酸乙酯必须使用的一种玻璃仪器是 。
(4)为充分利用反应物,提高乙酸乙酯产量,甲、乙两位同学分别设计了图8和图9两种装置(乙同学待反应完毕冷却后,再用饱和碳酸钠溶液提取烧瓶中的产物)。你认为效果较好的是 。
(5)若实验中用CH3CH218OH的乙醇与乙酸(CH3COOH)作用,此反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省高二下学期阶段测试5月 化学试卷(解析版) 题型:实验题
(14分)碳酸镁晶须是一种新型的吸波隐形材料中的增强材料。
(1)合成该物质的步骤如下:
步骤1:配制0.5 mol·L-1MgSO4溶液和0.5 mol·L-1NH4HCO3溶液。
步骤2:用量筒量取500 mL NH4HCO3溶液于1 000 mL三口烧瓶中,开启搅拌器。温度控制在50 ℃。
步骤3:将250 mL MgSO4溶液逐滴加入NH4HCO3溶液中,1 min内滴加完后,用氨水调节溶液pH到9.5。
步骤4:放置1 h后,过滤、洗涤。
步骤5:在40 ℃的真空干燥箱中干燥10 h,得碳酸镁晶须产品(MgCO3·nH2O n=1~5)。
回答下列问题:
步骤3中加氨水后的离子方程式 。
(2)测定合成的MgCO3·nH2O中的n值。称量1.000 g碳酸镁晶须,放入如图所示的广口瓶中加入水滴入稀硫酸与晶须反应,生成的CO2被NaOH溶液吸收,在室温下反应4~5 h,反应后期将温度升到30 ℃,最后的烧杯中的溶液用已知浓度的盐酸滴定,测得CO2的总量;重复上述操作2次。


①图中气球的作用是 。
②上述反应后期要升温到30℃,主要目的是 。
③用已知浓度的盐酸滴定烧杯中的溶液时应选用 为指示剂,若盛放盐酸的滴定管在滴定前有气泡未排尽,滴定后无气泡(其他操作均正确),则所测CO2的量会 (填“偏大”“偏小”“无影响”)
④设3次实验测得每1.000 g碳酸镁晶须与稀硫酸反应产生的CO2平均值为a mol,则n值为 (用含a的表达式表示)。
(3)称取100 g上述晶须产品进行热重分析,热重曲线如图。则该条件下合成的晶须中,n= (选填1、2、3、4、5)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com