



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢ŌŚĘÆ°×·ŪµÄČÜŅŗÖŠĶØČėÉŁĮ涞Ńõ»ÆĮņĘųĢå£ŗCa2++2ClO-+SO2+H2O=CaSO3+”ż2HClO | ||||
B”¢ÓƶčŠŌµē¼«µē½ā±„ŗĶŹ³ŃĪĖ®Cl-+H2O
| ||||
| C”¢ĀČ»ÆŃĒĢśČÜŅŗÖŠµĪČĖÉŁĮæĖ«ŃõĖ®2Fe2++2H++H2O2=2Fe3++2H2O | ||||
| D”¢µČĪļÖŹµÄĮæÅØ¶Č”¢µČĢå»żµÄCa£ØHCO3£©2ČÜŅŗÓėĒāŃõ»ÆÄĘČÜŅŗĻą»ģŗĻ£ŗCa2++2HCO3-=CaCO3”ż+CO32-+2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

 £©ŗĶ°¢Ė¾Ę„ĮÖÓŠĻąĖĘµÄ½į¹¹£¬ĖüµÄŅ»ÖÖÖʱø·½·ØČēĻĀ
£©ŗĶ°¢Ė¾Ę„ĮÖÓŠĻąĖĘµÄ½į¹¹£¬ĖüµÄŅ»ÖÖÖʱø·½·ØČēĻĀ
 Óė×ćĮæµÄĒāäåĖįŌŚ¼ÓČČĢõ¼žĻĀ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ
Óė×ćĮæµÄĒāäåĖįŌŚ¼ÓČČĢõ¼žĻĀ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

 ŗĶ»ÆŗĻĪļ¢ö£®
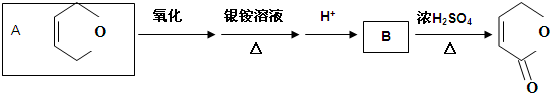
ŗĶ»ÆŗĻĪļ¢ö£® µÄŅ»ÖÖĶ¬·ÖŅģ¹¹Ģå¾Ńõ»ÆŗóŅ²ÄܵƵ½ÉĻŹö»ÆŗĻĪļ¢ń£¬øĆĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½ŹĒ
µÄŅ»ÖÖĶ¬·ÖŅģ¹¹Ģå¾Ńõ»ÆŗóŅ²ÄܵƵ½ÉĻŹö»ÆŗĻĪļ¢ń£¬øĆĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½ŹĒ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
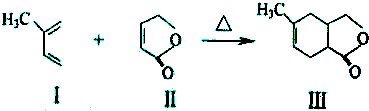
 ÓėCH”ŌCH£ØŅŅČ²£©Ņ²ÄÜ·¢ÉśDiels-Alder·“Ó¦£¬ĒėŠ“³öøĆ·“Ó¦²śĪļµÄ½į¹¹¼ņŹ½
ÓėCH”ŌCH£ØŅŅČ²£©Ņ²ÄÜ·¢ÉśDiels-Alder·“Ó¦£¬ĒėŠ“³öøĆ·“Ó¦²śĪļµÄ½į¹¹¼ņŹ½²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ¢ń |
| ¢ņ |
| µŖµÄ¹Ģ¶Ø |
| ||

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| Ź±¼ä/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c£ØNO£©/mol?L-1 | 1.00”Į10-3 | 4.50”Į10-4 | 2.50”Į10-4 | 1.50”Į10-4 | 1.00”Į10-4 | 1.00”Į10-4 |
| c£ØCO£©/mol?L-1 | 3.60”Į10-3 | 3.05”Į10-3 | 2.85”Į10-3 | 2.75”Į10-3 | 2.70”Į10-3 | 2.70”Į10-3 |
| c(NH4+) |
| c(SO42-) |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢ÓĶÖ¬ | B”¢ÕįĢĒ |
| C”¢ĘĻĢŃĢĒ | D”¢µ°°×ÖŹ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com