
| A.氢气2.24L | B.一氧化氮4.48L |
| C.氢气 4.48L | D.一氧化氮2.24L |
科目:高中化学 来源:不详 题型:单选题
 原产物全部是NO。向反应后的溶液中加入一定量的NaOH溶液,恰好使铁元素完全转化为沉淀,过滤,将滤渣洗涤、干燥、灼烧、称重,得固体a克,把滤液蒸干、灼烧、称重,得固体b克。
原产物全部是NO。向反应后的溶液中加入一定量的NaOH溶液,恰好使铁元素完全转化为沉淀,过滤,将滤渣洗涤、干燥、灼烧、称重,得固体a克,把滤液蒸干、灼烧、称重,得固体b克。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.80mL l mol·L-1的稀硝酸溶液 | B.80mL 0.5mol·L-1的稀盐酸 |
| C.80mL lmnl·L-1的FeCI3溶液 | D.80mL 0.5mol·L-l的稀硫酸溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 列问题:
列问题:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.40.32L | B.30.24L | C.20.16L | D.6.72L |
 不可行,请说明原因。若可行,请写出反应的离子方程式: 。
不可行,请说明原因。若可行,请写出反应的离子方程式: 。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 学方程式为 ;
学方程式为 ;
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
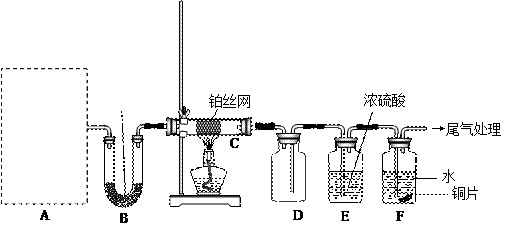
 检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯。部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解。
检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯。部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
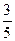 ,则混合气体中N2与NO2的体积比是
,则混合气体中N2与NO2的体积比是| A.2:3 | B.3:2 | C.3:5 | D.5:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com