

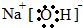 ,
,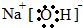 ;
;

科目:高中化学 来源: 题型:
| A、固氮就是把氮元素转化为固体 |
| B、FeSO4溶液保存在加有少量铁粉的试剂瓶中 |
| C、浓硝酸保存在具磨口玻璃塞的无色试剂瓶中 |
| D、碳酸氢铵潮解后可以在太阳底下暴晒至干 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向Al2(SO4)3溶液中滴入过量的氨水,先有白色沉淀产生,后沉淀溶解 |
| B、向品红试液中通入SO2后溶液由红色褪为无色,加热后又变红色 |
| C、浓盐酸、浓硝酸和浓硫酸长期暴露在空气中浓度都会降低 |
| D、向饱和碳酸钠溶液中通入二氧化碳,溶液变浑浊 |
查看答案和解析>>
科目:高中化学 来源: 题型:
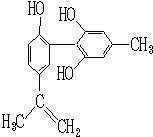 我国支持“人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
我国支持“人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )| A、该有机物遇FeCl3溶液呈紫色 |
| B、该分子中的所有碳原子一定在同一个平面上 |
| C、滴入酸性KMnO4溶液,观察紫色褪去,能证明结构中存在碳碳双键 |
| D、1mol该物质分别与浓溴水和H2反应,最多消耗Br2和H2的物质的量分别为4mol、7mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
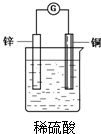 把一块锌片和一块铜片平行地插入盛有稀硫酸溶液的烧杯中,观察到的现象是
把一块锌片和一块铜片平行地插入盛有稀硫酸溶液的烧杯中,观察到的现象是查看答案和解析>>
科目:高中化学 来源: 题型:
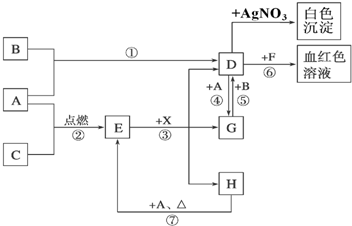
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| n[(CN)2]/mol | 0.1 | 0.2 | 0.3 |
| c(SCN-)/mol?L-1 | 2 | a | 0 |
| c(Br-)/mol?L-1 | 1 | 1 | 1 |
| c(I-)/mol?L-1 | 1 | 0 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间 | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4) | 0.100 | c1 | 0.050 | c3 | a | b |
| c(NO2) | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com