
 ĀČŌŖĖŲµÄµ„ÖŹ¼°Ęä»ÆŗĻĪļŌŚÉś²śÉś»īÖŠ¶¼ŗÜÖŲŅŖ£®»Ų“šĻĀĮŠĪŹĢā£ŗ
ĀČŌŖĖŲµÄµ„ÖŹ¼°Ęä»ÆŗĻĪļŌŚÉś²śÉś»īÖŠ¶¼ŗÜÖŲŅŖ£®»Ų“šĻĀĮŠĪŹĢā£ŗ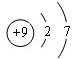 £®
£®·ÖĪö £Ø1£©ÓėĀČŌŖĖŲĶ¬×åµÄ¶ĢÖÜĘŚŌŖĖŲĪŖF£»
£Ø2£©ÓėĀČŌŖĖŲĶ¬ÖÜĘŚµÄĄė×Ó°ė¾¶×īŠ”µÄŌŖĖŲµÄµ„ÖŹŹĒĀĮ£¬¹¤ŅµÓƵē½āŃõ»ÆĀĮµÄ·½·ØŅ±Į¶ĀĮ£¬¼ÓČė±ł¾§ŹÆæɽµµĶČŪµć£»
£Ø3£©Ä³ĢžŌŚŅ»¶ØĢõ¼žĻĀŗĶĀČĘų·“Ӧɜ³É1£¬2-¶žĀČ-3£¬3-¶ž¼×»łĪģĶ飬C=C»ņC”ŌCÖ»ÄÜĪ»ÓŚ1”¢2CŌ×ÓÖ®¼ä£»
£Ø4£©¢Łµē½āŹ±£¬Ńō¼«ÉĻĀČĄė×ӷŵēÉś³ÉĀČĖįøłĄė×Ó”¢Ņõ¼«ÉĻĒāĄė×ӷŵēÉś³ÉĒāĘų£»
¢ŚĮ½ÖÖ»ÆŗĻĪļĻą»„½»»»³É·ÖÉś³ÉĮķĶāµÄĮ½ÖÖ»ÆŗĻĪļµÄ·“Ó¦ĪŖø“·Ö½ā·“Ó¦£¬ĻąĶ¬ĪĀ¶ČĻĀ£¬Čܽā¶ČŠ”µÄĪļÖŹĻČĪö³ö£»
£Ø5£©Ņ»¶ØĢõ¼žĻĀ£¬ŌŚĖ®ČÜŅŗ1 mol Cl-”¢ClOx-£Øx=1£¬2£¬3£¬4£¬£©µÄÄÜĮæ£ØkJ£©Ļą¶Ō“óŠ”ČēĶ¼ĖłŹ¾£®
¢ŁDÖŠClŌŖĖŲ»ÆŗĻ¼ŪĪŖ+7¼Ū£¬¾Ż“ĖÅŠ¶ĻxÖµ£»
¢ŚB”śA+C£¬øł¾Ż×ŖŅʵē×ÓŹŲŗćµĆøĆ·“Ó¦·½³ĢŹ½ĪŖ3ClO-=ClO3-+2Cl-£¬·“Ó¦ČČ=£Ø63kJ/mol+2”Į0kJ/mol£©-3”Į60kJ/mol=-117kJ/mol£®
½ā“š ½ā£ŗ£Ø1£©ÓėClĶ¬Ņ»Ö÷×åŹĒ¶ĢÖÜĘŚŌŖĖŲŹĒFŌŖĖŲ£¬FŌ×ÓŗĖĶāÓŠ2øöµē×Ó²ć”¢×īĶā²ć7øöµē×Ó£¬ĘäŌ×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ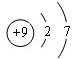 £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ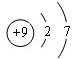 £»
£»
£Ø2£©ÓėĀČŌŖĖŲĶ¬ÖÜĘŚµÄĄė×Ó°ė¾¶×īŠ”µÄŌŖĖŲµÄµ„ÖŹŹĒĀĮ£¬¹¤ŅµÓƵē½āŃõ»ÆĀĮµÄ·½·ØŅ±Į¶ĀĮ£¬¼ÓČė±ł¾§ŹÆæɽµµĶČŪµć£¬µē½āŹ±Ńō¼«²ÄĮĻŅŖ¶ØĘŚøü»»£¬ŌŅņŹĒŃō¼«ŹÆÄ«ŌŚøßĪĀĻĀÓėŃō¼«²śÉśµÄŃõĘų·¢Éś·“Ó¦¶ųĻūŗÄ£¬
¹Ź“š°øĪŖ£ŗAl£»ČŪ¼Į£»Ńō¼«ŹÆÄ«ŌŚøßĪĀĻĀÓėŃō¼«²śÉśµÄŃõĘų·¢Éś·“Ó¦¶ųĻūŗÄ£»
£Ø3£©Ä³ĢžŌŚŅ»¶ØĢõ¼žĻĀŗĶĀČĘų·“Ӧɜ³É1£¬2-¶žĀČ-3£¬3-¶ž¼×»łĪģĶ飮
¢ŁČē¹ūøĆĢžŹĒĻ©Ģž£¬ŌņæÉÄܵĽį¹¹¼ņŹ½ŹĒCH2=CH-C£ØCH3£©2-CH2CH3£¬¹Ź“š°øĪŖ£ŗCH2=CH-C£ØCH3£©2-CH2CH3£»
¢ŚČē¹ūøĆĢžŹĒČ²Ģž£¬ŌņæÉÄܵĽį¹¹¼ņŹ½ŹĒHC”ŌC-C£ØCH3£©2-CH2CH3£¬¹Ź“š°øĪŖ£ŗHC”ŌC-C£ØCH3£©2-CH2CH3£»
¢ŪøĆĢž¼ÓĒāŗóÉś³ÉĪļµÄĶ¬·ÖŅģ¹¹MµÄŅ»ĀČ“śĪļÓŠ3ÖÖ£¬Ó¦ĪŖCH3CH£ØCH3£©CH2CH£ØCH3£©CH3£¬ŌņMµÄĆū³ĘŹĒ2£¬4-¶ž¼×»łĪģĶ飬¹Ź“š°øĪŖ£ŗ2£¬4-¶ž¼×»łĪģĶ飻
£Ø4£©¢Łµē½āŹ±£¬Ńō¼«ÉĻĀČĄė×ӷŵēÉś³ÉĀČĖįøłĄė×Ó”¢Ņõ¼«ÉĻĒāĄė×ӷŵēÉś³ÉĒāĘų£¬ĖłŅŌ·“Ó¦·½³ĢŹ½ĪŖNaCl+3H2O$\frac{\underline{\;µē½ā\;}}{\;}$NaClO3+3H2”ü£¬
¹Ź“š°øĪŖ£ŗNaCl+3H2O$\frac{\underline{\;µē½ā\;}}{\;}$NaClO3+3H2”ü£»
¢ŚNaClO3×Ŗ»ÆĪŖKClO3£¬ĖµĆ÷øĆ·“Ó¦ÖŠĮ½ÖÖĪļÖŹĻą»„½»»»Ąė×ÓÉś³ÉŃĪ£¬ĪŖø“·Ö½ā·“Ó¦£¬ĻąĶ¬ĪĀ¶ČĻĀ£¬Čܽā¶ČŠ”µÄĪļÖŹĻČĪö³ö£¬ŹŅĪĀĻĀKClO3ŌŚĖ®ÖŠµÄČܽā¶ČĆ÷ĻŌŠ”ÓŚĘäĖü¾§Ģ壬ĖłŅŌĻČĪö³öKClO3£»
¹Ź“š°øĪŖ£ŗø“·Ö½ā·“Ó¦£»ŹŅĪĀĻĀ£¬ĀČĖį¼ŲŌŚĖ®ÖŠµÄČܽā¶ČĆ÷ĻŌŠ”ÓŚĘäĖū¾§Ģ壻
£Ø4£©¢Łøł¾ŻĶ¼ĻóÖŖ£¬DÖŠClŌŖĖŲ»ÆŗĻ¼ŪĪŖ+7¼Ū£¬ĖłŅŌClOx-ÖŠxĪŖ4£¬ŌņDĪŖClO4-£»
¹Ź“š°øĪŖ£ŗClO4-£»
¢ŚB”śA+C·¢Éś·“Ó¦£ŗ3 ClO-=ClO3-+2Cl-£¬øł¾ŻĄė×ÓÄÜĮææÉÖŖ£¬·“Ó¦ČČ”÷H=53kJ/mol+2”Į0kJ/mol-3”Į60kJ/mol=-117kJ/mol£¬¹Ź·“Ó¦ČČ»Æѧ·½³ĢŹ½ĪŖ£ŗ3ClO-£Øaq£©ØTClO3-£Øaq£©+2Cl-£Øaq£©”÷H=-117kJ/mol£¬
¹Ź“š°øĪŖ£ŗ3ClO-£Øaq£©ØTClO3-£Øaq£©+2Cl-£Øaq£©”÷H=-117kJ/mol£®
µćĘĄ ±¾Ģāæ¼²é½Ļ×ŪŗĻ£¬Éę¼°Ō×Ó½į¹¹”¢ĪļÖŹŠŌÖŹ”¢ŌŖĖŲÖÜĘŚĀÉ”¢øĒĖ¹¶ØĀɵÄÓ¦ÓĆ”¢µē×ÓŹ½µČÖŖŹ¶µć£¬Ķ¬Ź±æ¼²éѧɜ·ÖĪöĪŹĢā”¢½ā“šĪŹĢāÄÜĮ¦£¬ÖŖµĄ½šŹōŠŌ”¢·Ē½šŹōŠŌĒæČõÅŠ¶Ļ·½·Ø£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
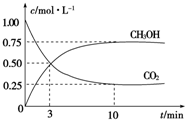 2009Äź12ŌĀ7ČÕÖĮ18ČÕ£¬Ęųŗņ±ä»Æ·å»įŌŚµ¤ĀóŹ×¶¼øē±¾¹žøłÕŁæŖ£¬½ŚÄܼõÅųÉĪŖ»įŅéµÄÖŲŅŖŅéĢā£®ČēŗĪ½µµĶ“óĘųÖŠCO2µÄŗ¬Įæ¼°ÓŠŠ§µŲæŖ·¢ĄūÓĆCO2£¬ŅżĘšĮĖø÷¹śµÄĘÕ±éÖŲŹÓ£®ÄæĒ°¹¤ŅµÉĻÓŠŅ»ÖÖ·½·ØŹĒÓĆCO2Ą“Éś²śČ¼ĮĻ¼×“¼£®ĪŖĢ½¾æ·“Ó¦ŌĄķ£¬ĻÖ½ųŠŠČēĻĀŹµŃ飬ŌŚĢå»żĪŖ1LµÄĆܱÕČŻĘ÷ÖŠ£¬³äČė1mol CO2ŗĶ3mol H2£¬Ņ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦£ŗCO2£Øg£©+3H2£Øg£©?CH3OH£Øg£©+H2O£Øg£©£® ²āµĆCO2ŗĶCH3OH£Øg£©µÄÅضČĖꏱ¼ä±ä»ÆČēĶ¼ĖłŹ¾£®
2009Äź12ŌĀ7ČÕÖĮ18ČÕ£¬Ęųŗņ±ä»Æ·å»įŌŚµ¤ĀóŹ×¶¼øē±¾¹žøłÕŁæŖ£¬½ŚÄܼõÅųÉĪŖ»įŅéµÄÖŲŅŖŅéĢā£®ČēŗĪ½µµĶ“óĘųÖŠCO2µÄŗ¬Įæ¼°ÓŠŠ§µŲæŖ·¢ĄūÓĆCO2£¬ŅżĘšĮĖø÷¹śµÄĘÕ±éÖŲŹÓ£®ÄæĒ°¹¤ŅµÉĻÓŠŅ»ÖÖ·½·ØŹĒÓĆCO2Ą“Éś²śČ¼ĮĻ¼×“¼£®ĪŖĢ½¾æ·“Ó¦ŌĄķ£¬ĻÖ½ųŠŠČēĻĀŹµŃ飬ŌŚĢå»żĪŖ1LµÄĆܱÕČŻĘ÷ÖŠ£¬³äČė1mol CO2ŗĶ3mol H2£¬Ņ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦£ŗCO2£Øg£©+3H2£Øg£©?CH3OH£Øg£©+H2O£Øg£©£® ²āµĆCO2ŗĶCH3OH£Øg£©µÄÅضČĖꏱ¼ä±ä»ÆČēĶ¼ĖłŹ¾£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
 ĻÖÓŠ“æĢśĘ¬”¢“æŅųʬ”¢“æĶʬ£¬Ļ”ĮņĖį”¢FeSO4 ČÜŅŗ”¢Fe2£ØSO4£©3ČÜŅŗ”¢“óÉÕ±”¢µ¼ĻßČōøÉ£¬ĒėŌĖÓĆŌµē³ŲŌĄķÉč¼ĘŹµŃ飬ŃéÖ¤Cu2+”¢Fe3+µÄŃõ»ÆŠŌĒæČõ£®
ĻÖÓŠ“æĢśĘ¬”¢“æŅųʬ”¢“æĶʬ£¬Ļ”ĮņĖį”¢FeSO4 ČÜŅŗ”¢Fe2£ØSO4£©3ČÜŅŗ”¢“óÉÕ±”¢µ¼ĻßČōøÉ£¬ĒėŌĖÓĆŌµē³ŲŌĄķÉč¼ĘŹµŃ飬ŃéÖ¤Cu2+”¢Fe3+µÄŃõ»ÆŠŌĒæČõ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ö»ŅŖŹĒŃõ»Æ»¹Ō·“Ó¦ŌĄķ¶¼æÉŅŌÉč¼Ę³ÉŌµē³Ų | |
| B£® | Cu+2H+ØTCu2++H2”üŌŚČĪŗĪĢõ¼žĻĀ¶¼²»ÄܽųŠŠ | |
| C£® | ½šŹōµÄ·Ą»¤æÉŅŌ²ÉČ”ÖĘ³ÉŗĻ½š£¬øıäÄŚ²æ½į¹¹µÄ·½·Ø | |
| D£® | ĻÖ“śĒ±Ķ§µÄ·ĄøÆŹĒŌŚĒ±Ķ§µ×²æĢłŠæ°å |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
| ŃōĄė×Ó | K+”¢Ag+”¢Mg2+”¢Ba2+ |
| ŅõĄė×Ó | NO3-”¢CO32-”¢SiO32-”¢SO42- |
| ŠņŗÅ | ŹµŃéÄŚČŻ | ŹµŃé½į¹ū |
| ¢ń | ĻėøĆČÜŅŗÖŠ¼ÓČė×ćĮæĻ”ŃĪĖį | Éś³É°×É«³Įµķ²¢ŌŚ±ź×¼×“æöĻĀ·Å³ö0.56LĘųĢå |
| ¢ņ | ½«¢ńÖŠ²śÉśµÄ»ģŗĻŅŗ¹żĀĖ£¬½«³ĮµķĻ“µÓ”¢×ĘÉÕÖĮŗćÖŲ£¬³ĘĮæĖłµĆ¹ĢĢåµÄÖŹĮæ | ¹ĢĢåÖŹĮæĪŖ2.4g |
| ¢ó | Ļņ¢ņÖŠĖłµĆµÄĀĖŅŗÖŠµĪ¼ÓBaCl2ČÜŅŗ | ĪŽĆ÷ĻŌĻÖĻó |
| ŅõĄė×Ó | NO3- | CO32- | SiO32- | SO42- |
| c/mol•L-1 | £æ | 0.25mol/L | 0.4mol/L | 0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĮņĖįÓėĒāŃõ»Æ±µ·“Ó¦£ŗBa2++OH-+H++SO42-ØTBaSO4”ż+H2O | |
| B£® | ¶žŃõ»ÆĢ¼Óė×ćĮæµÄĒāŃõ»ÆÄĘ·“Ó¦£ŗCO2+2OH-ØTCO32-+H2O | |
| C£® | “óĄķŹÆÓėŃĪĖį·“Ó¦£ŗCO32-+2H+ØTH2O+CO2”ü | |
| D£® | ĢśÓėĻ”ĮņĖį·“Ó¦£ŗ2Fe+6H+ØT2Fe3++3H2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 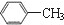 | B£® | H2CØTCH-CH3 | C£® |  | D£® | 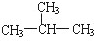 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  1£¬4-¶ž¼×»ł¶” 1£¬4-¶ž¼×»ł¶” | B£® | 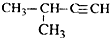 3-¼×»ł¶”Č² 3-¼×»ł¶”Č² | C£® | 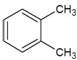 ¶ž¼×»ł±½ ¶ž¼×»ł±½ | D£® | 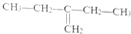 2-ŅŅ»ł-1-¶”Ļ© 2-ŅŅ»ł-1-¶”Ļ© |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com