
下列叙述正确的是( )
A.氯气的性质很活泼,它与氢气混合后立即发生爆炸
B.可以用氢氧化钙溶液吸收实验室制取氯气时多余的氯气
C.检验Cl2气体中是否混有HCl方法是将气体通入硝酸银溶液
D.除去Cl2气体中的HC l,可将气体通入饱
l,可将气体通入饱 和食盐水
和食盐水
科目:高中化学 来源: 题型:
甲醇又称“木醇”或“木精”,沸点64.7℃,是无色有酒精气味易挥发的液体。甲醇有毒,误饮5~10mL能双目失明,大量饮用会导致死亡。甲醇是重要的化学工业基础原料和液体燃料,可用于制造甲醛和农药,并常用作有机物的萃取剂和酒精的变性剂等。
⑴工业上可利用CO2和H2生产甲醇,方程式如下:
CO2(g)+3H2(g)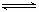 CH3OH(l)+H2O (g) △H=Q1kJ·mol-1
CH3OH(l)+H2O (g) △H=Q1kJ·mol-1
又查资料得知:①CH3OH(l)+1/2 O2(g)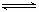 CO2(g)+2H2(g) △H=Q2kJ·mol-1
CO2(g)+2H2(g) △H=Q2kJ·mol-1
②H2O(g)=H2O(l) △H= Q3kJ·mol-1,则表示甲醇的燃烧热的热化学方程式为 。
⑵工业上可用CO和H2O (g) 来合成CO2 和H2,再利用⑴中反应原理合成甲醇。某温度下,将1molCO和1.5molH2O充入10 L固定密闭容器中进行化学反应:
L固定密闭容器中进行化学反应:
CO(g)+H2O(g)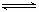 CO2(g)+H2(g) △H>0,当反应进行到10min时达到平衡,此时测得H2为0.6 mol。回答下列问题:
CO2(g)+H2(g) △H>0,当反应进行到10min时达到平衡,此时测得H2为0.6 mol。回答下列问题:
①0~10min内H2O(g)的平均反应速率为 。
②若想加快正反应速率的同时提高CO的转化率,可以采用的方法 是 。
是 。
a.升高温度 b.缩小容器的体积
c.增大H2O (g)的浓度 d.加入适当的催化剂
③若保持温度容积不变再向其中充入1molCO和0.5molH2O(g),重新达到化学平衡状态时,此时平衡混合气体中H2的体积分数为 。
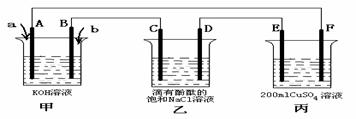
⑶甲醇燃料电池是符合绿色化学理念的新型燃料电池,下图是以甲醇燃料电池(甲池)为电源的电解装置。已知:A、B、C、D、E、F都是惰性电极,丙中为0.1 mol/L CuSO4溶液 (假设反应前后溶液体积不变) ,当向甲池通入气体a和b时,D极附近呈红色。回答下列问题:
① a物质是 , A电极的电极反应式为 。
② 乙装置中的总化学反应方程式为 。
③ 当乙装置中C电极收集到224mL(标况下)气体时, 丙中溶液的pH= 。
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,浓度都是1 mol·L-1的两种气体X2和Y2,在密闭容器中反应生成气体Z,经过t min后,测得物质的浓度分别为:[X2]=0.4 mol·L-1,[Y2]=0.8 mol·L-1,[Z]=0.4 mol·L-1,则该反应的反应式可表示为( )
A.X2+2Y2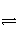
 2XY2 B.2X2+Y2
2XY2 B.2X2+Y2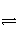
 X2Y
X2Y
C.3X2+Y2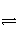
 2X3Y D.X2+3Y2
2X3Y D.X2+3Y2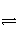
 2XY3
2XY3
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学—选修5:有机化学基础】A是一取代芳香化合物,相对分子质量为136,分子中只含碳、氢、氧,其中氧的含量为23.5%。实验表明: A的芳环侧链上只含一个官能团;A和NaOH溶液反应后酸化可以得到E(C7H6O2)和F。
(1)A、E、F的结构简式。
(2)A和NaOH溶液反应、酸化的实验装置如下:
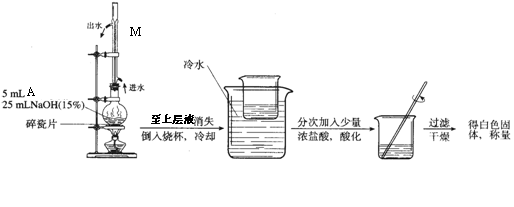

 写出A与NaOH溶液反应的化学反应方程式 。
写出A与NaOH溶液反应的化学反应方程式 。
写出实验装置中M的名称和作用 。
(3)A有多种同分异构体,符合下列条件的结构共有 种,
①可以发生银镜反应 ②属于芳香族化合物,不具备其它环状结构
③可以与氢氧化钠溶液反应 ④不能与FeCl3发生显色反应
请写出其中核磁共振氢谱有5个吸收峰的A的结构的结构简式:
查看答案和解析>>
科目:高中化学 来源: 题型:
.已知酸性: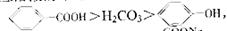 综合考虑反应物的转化率和原料成本等
综合考虑反应物的转化率和原料成本等
因素,将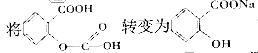 的最佳方法是
的最佳方法是
A.与稀H2SO4共热后,加入足量NaOH溶液
B.与稀H2SO4共热后,加入足量溶液
C.与足量的NaOH溶液共热后,再加入适量H2SO4
D.与足量的NaOH溶液共热后,再通入足量CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于氯水的叙述,不正确的是( )
A.新制氯水中只含Cl2和H2O分子
B.新制氯水可使蓝色石蕊试纸先变红后褪色
C.光照氯水有气泡逸出,该气体是O2
D.氯水放置后溶液的酸性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
①氯气的性质活泼,它与氢气混合后立即发生爆炸
②实验室制取氯气时,为了防止环境污染,多余的氯气可以用氢氧化钙溶液吸收
③新制氯水的氧化性强于久置氯水
④检验HCl气体中是否混有Cl2方法是将气体通入硝酸银溶液
⑤除去HCl气体中的Cl2,可将气体通入饱和食盐水
A.① ② ③ B.② ③ ④ C.③ D.③ ⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
丙烯酸乙酯(化合物Ⅳ)是制备塑料、树脂等高聚物的重要中间体,可由下面路线合成:
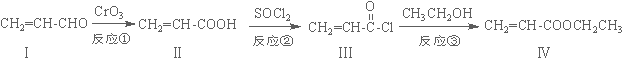 (1)化合物Ⅳ的分子式为 ,1 mol化合物Ⅳ完全燃烧消耗O2为 mol。
(1)化合物Ⅳ的分子式为 ,1 mol化合物Ⅳ完全燃烧消耗O2为 mol。
(2)化合物Ⅱ能使溴水褪色,其反应方程式为 。
(3)反应②属于 反应,化合物Ⅰ可以由化合物Ⅴ(分子式为C3H6O)催化氧化得到,则化合物Ⅴ→Ⅰ的反应方程式为 。
(4)化合物Ⅵ是化合物Ⅳ的同分异构体,Ⅵ含有碳碳双键并能与NaHCO3溶液反应放出气体,其核磁共振氢谱峰面积之比为1:1:6,则化合物Ⅵ的结构简式为 。
(5)一定条件下,化合物  也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为 。
也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y是主族元素,I为电离能,单位是kJ·mol-1。请根据下表所列数据判断,下列说法错误的是( )
| 电离能/kJ·mol-1 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4600 | 6900 | 9500 |
| Y | 580 | 1800 | 2700 | 11 |
A.元素X的常见化合价是+1价
 B.元素Y是第ⅢA族元素
B.元素Y是第ⅢA族元素
C.元素X与氯形成化合物时,化学式可能是XCl
D.若元素Y处于第三周期,则它可与冷水剧烈反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com