
【题目】下列说法不正确的是![]()
![]()
A. ![]() 、
、![]() 的晶体结构类型不同
的晶体结构类型不同
B. 加热硅、硫晶体使之熔化,克服的作用力不同
C. HCl、NaCl溶于水,破坏的化学键类型相同
D. NaOH、![]() 晶体中既有离子键又有共价键
晶体中既有离子键又有共价键
【答案】C
【解析】A项,CO2属于分子晶体,SiO2属于原子晶体;B项,硅晶体属于原子晶体,硫晶体属于分子晶体;C项,HCl中含共价键,NaCl中含离子键;D项,NaOH、NH4Cl晶体中既有离子键又有共价键。
A项,CO2属于分子晶体,SiO2属于原子晶体,CO2、SiO2晶体结构类型不同,A项正确;B项,硅晶体属于原子晶体,加热硅晶体使之熔化克服共价键,硫晶体属于分子晶体,加热硫晶体使之熔化克服分子间作用力,加热硅、硫晶体使之熔化时克服的作用力不同,B项正确;C项,HCl中含共价键,HCl溶于水破坏共价键,NaCl中含离子键,NaCl溶于水破坏离子键,HCl、NaCl溶于水破坏的化学键类型不同,C项错误;D项,NaOH的电子式为![]() ,NH4Cl的电子式为
,NH4Cl的电子式为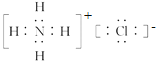 ,NaOH、NH4Cl晶体中既有离子键又有共价键,D项正确;答案选C。
,NaOH、NH4Cl晶体中既有离子键又有共价键,D项正确;答案选C。


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是
A. 10 g的D2O中含有的质子数与中子数分别为5NA和4NA
B. 常温下56g铁片投入足量浓H2SO4中生成1.5NA个SO2分子
C. 常温下,22gCO2和N2O混合气体中,含有的原子数目为1.5NA
D. pH=1的H3PO4溶液中,含有0.1NA个H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中产生气泡最快的是 ( )
温度 | 浓度 | 催化剂 | |
A | 25 ℃ | 2 mL 5% H2O2 | 0.1 mol·L-1 FeCl3 2滴 |
B | 35 ℃ | 2 mL 8% H2O2 | MnO2粉末 |
C | 25 ℃ | 2 mL 5% H2O2 | MnO2粉末 |
D | 25 ℃ | 2 mL 8% H2O2 | 无 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关元素或者化合物性质的比较中,正确的是![]()
![]()
A. 结构相似的分子晶体的熔沸点,与相对分子质量呈正相关,所以![]()
B. Na、Mg、Al原子最外层电子数依次增多,原子半径也依次增大
C. 在分子中,两个原子间的键长越长,键能越大
D. 一般而言,晶格能越高,离子晶体的熔点越高、硬度越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯仿![]() 常因保存不慎而被氧化,产生剧毒物光气
常因保存不慎而被氧化,产生剧毒物光气![]() :
:![]() ,下列说法不正确的有
,下列说法不正确的有![]()
![]()

A. ![]() 分子为含极性键的非极性分子
分子为含极性键的非极性分子
B. ![]() 分子中含有3个
分子中含有3个![]() 键、一个
键、一个![]() 键,中心C原子采用
键,中心C原子采用![]() 杂化
杂化
C. ![]() 分子中所有原子的最外层电子都满足8电子稳定结构
分子中所有原子的最外层电子都满足8电子稳定结构
D. 使用前可用硝酸银稀溶液检验氯仿是否变质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各种说法中不正确的是![]()
![]()
A. 在水中氢、氧原子间均以共价键相结合
B. 离子键是阳离子、阴离子的静电作用
C. ![]() 和
和![]() 的反应过程涉及了共价键的断裂和形成
的反应过程涉及了共价键的断裂和形成
D. 金属具有金属光泽及良好的导电性和导热性,这些性质均与金属键有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂-空气电池原理模型如图所示,下列说法不正确的是

A. 电池正极可以吸附空气中氧气作为氧化剂
B. 正极反应为2Li+ + O2 + 2e- ![]() Li2O2
Li2O2
C. 电解质能传递锂离子和电子,不可以用水溶液
D. 负极反应Li - e-=Li+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用所学化学知识解答问题:
![]() 在高温下CuO能分解生成
在高温下CuO能分解生成![]() ,试从原子结构角度解释其原因: ______
,试从原子结构角度解释其原因: ______ ![]() 根据元素原子的外围电子排布特征,可将周期表分成五个区域,元素Cu属于 ______ 区
根据元素原子的外围电子排布特征,可将周期表分成五个区域,元素Cu属于 ______ 区![]()
![]() 氰酸
氰酸![]() 是一种链状分子,它与异氰酸
是一种链状分子,它与异氰酸![]() 互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式 ______
互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式 ______ ![]() 其中的C的杂化类型为 ______ .
其中的C的杂化类型为 ______ .
![]() 原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物
原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物![]() 与Fe原子或离子形成配合物的分子或离子应具备的结构特征是 ______ .
与Fe原子或离子形成配合物的分子或离子应具备的结构特征是 ______ .
![]() 立方氮化硼是一种新型的超硬、耐磨、耐高温的结构材料,其晶胞结构与金刚石类似,一个该晶胞中含有 ______ 个氮原子, ______ 个硼原子,设氮原子半径为apm,硼的原子半径bpm,求该晶胞的空间利用率 ______
立方氮化硼是一种新型的超硬、耐磨、耐高温的结构材料,其晶胞结构与金刚石类似,一个该晶胞中含有 ______ 个氮原子, ______ 个硼原子,设氮原子半径为apm,硼的原子半径bpm,求该晶胞的空间利用率 ______ ![]() 用含a、b的代数式表示
用含a、b的代数式表示![]()

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com