
 ;与甲分子具有相同电子数且含元素种类相同的离子有(填化学式):OH-、H3O+.
;与甲分子具有相同电子数且含元素种类相同的离子有(填化学式):OH-、H3O+. Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀.
Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀. 分析 X、Y、Z、M四种短周期元素的原子半径依次减小.甲、乙、丙是由它们形成的三种常见分子;甲是人体必需的基本营养物质之一,约占人体体重的2/3,甲为水,可推知M为H元素;丙是具有强氧化性的弱酸,则丙为HClO,乙是日常生活的基础能源,其中含元素Y的质量分数为75%,乙为甲烷,可推知X为Cl、Y为C元素、Z为O元素;丁为丙的钠盐,常用于漂白或消毒,则丁为NaClO;戊与甲的组成元素相同,其分子具有18电子,则戊为H2O2,据此解答.
解答 解:X、Y、Z、M四种短周期元素的原子半径依次减小.甲、乙、丙是由它们形成的三种常见分子;甲是人体必需的基本营养物质之一,约占人体体重的2/3,甲为水,可推知M为H元素;丙是具有强氧化性的弱酸,则丙为HClO,乙是日常生活的基础能源,其中含元素Y的质量分数为75%,乙为甲烷,可推知X为Cl、Y为C元素、Z为O元素;丁为丙的钠盐,常用于漂白或消毒,则丁为NaClO;戊与甲的组成元素相同,其分子具有18电子,则戊为H2O2.
(1)元素X、Y的最高价氧化物的水化物分别为:HClO4、H2CO3,非金属性Cl>C,故酸性由强到弱为HClO4>H2CO3;丁为NaClO,电子式为  ;与甲(水)分子具有相同电子数且含元素种类相同的离子有:OH-、H3O+,
;与甲(水)分子具有相同电子数且含元素种类相同的离子有:OH-、H3O+,
故答案为:HClO4>H2CO3; ;OH-、H3O+;
;OH-、H3O+;
(2)元素E、F与X(Cl)同周期.
①常温下E的单质与甲反应缓慢,加热至沸反应迅速,滴加酚酞试液,溶液变红色,则E为Mg,此反应的化学方程式为Mg+2H2O$\frac{\underline{\;△\;}}{\;}$ Mg(OH)2+H2↑,
故答案为:Mg+2H2O$\frac{\underline{\;△\;}}{\;}$ Mg(OH)2+H2↑;
②F的单质粉末加油漆后即得“银粉漆”,则F为Al,易与氧气反应,与酸、碱反应,保存“银粉”时的注意密封、避免与酸或碱接触;
故答案为:密封;避免与酸或碱接触;
(3)①过氧化氢具有强氧化性,将亚铁离子氧化为铁离子,反应的离子方程式:2Fe2++H2O2+2H+=2Fe3++2H2O,故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
②过氧化氢在铁离子作催化剂条件下分解生成水与氧气,反应方程式为:2H2O2 $\frac{\underline{\;Fe_{3}+\;}}{\;}$2H2O+O2↑,
故答案为:2H2O2 $\frac{\underline{\;Fe_{3}+\;}}{\;}$2H2O+O2↑;
③起始反应即①中使c(H+)降低,且反应②放热,使Fe3++3H2O Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀,
Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀,
故答案为:起始反应即①中使c(H+)降低,且反应②放热,使Fe3++3H2O Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀.
Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀.
点评 本题考查元素化合物推断,是对学生综合能力的考查,需要学生熟练注意元素化合物知识,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 一定条件下2molSO2和1molO2充分反应后,混合气体的分子总数大于2NA | |
| B. | 常温常压下,64gO2和O3混合气体中含有原子总数为4NA | |
| C. | 1molCl2与NaOH溶液反应,转移的电子总数为2NA | |
| D. | 标准状况下,22.4LN2含共用电子对数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
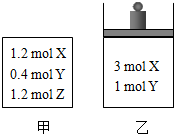 在温度、初始容积相同的两个密闭容器中,按不同方式投入反应物(如图所示),发生如下反应:3X(g)+Y(g)?2Z(g)△H<0,保持温度不变,测得平衡时的有关数据如下:下列说法正确的是( )
在温度、初始容积相同的两个密闭容器中,按不同方式投入反应物(如图所示),发生如下反应:3X(g)+Y(g)?2Z(g)△H<0,保持温度不变,测得平衡时的有关数据如下:下列说法正确的是( )| 恒容容器甲 | 恒压容器乙 | |
| Y的物质的量/mol | n1 | n2 |
| Z的体积分数 | φ1 | φ2 |
| A. | 平衡时容器乙的容积一定比反应前大 | |
| B. | 平衡时容器甲的压强一定比反应前大 | |
| C. | n2>n1 | |
| D. | φ2>φ1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Z | |
| Y |
| A. | 原子半径:X>Y>Z | B. | 气态氢化物稳定性:X<Y<Z | ||
| C. | 元素的非金属性强弱:Y<X<Z | D. | Y和Z形成的是分子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
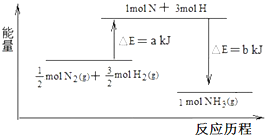 在化学反应中,反应物转化成生成物,必然发生能量的变化.
在化学反应中,反应物转化成生成物,必然发生能量的变化.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃和l00℃时H2O的KW | |
| B. | 同温同浓度的KHCO3溶液和NH4HCO3,溶液中的c(HCO3-) | |
| C. | 同温同浓度的NaHCO3溶液和CH3COONa溶液的pH | |
| D. | 中和25mL0.1mol/L NaOH溶液所需CH3COOH和HCl的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | ||
| Z | W |
| A. | X位于元素周期表中第2周期、第VA族 | |
| B. | Y的氢化物(H2Y)不稳定,100℃以上即可分解 | |
| C. | W的非金属性比Y的非金属性弱 | |
| D. | Z的最高价氧化物的水化物是一种强碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
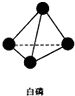 ,并指出1mol白磷(P4)含有P-P键的数目6NA
,并指出1mol白磷(P4)含有P-P键的数目6NA查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com