
| A. | 分子晶体中一定含有共价键 | |
| B. | 离子晶体中一定含有离子键 | |
| C. | 含有极性键的分子一定是极性分子 | |
| D. | 含有非极性键的分子一定是非极性分子 |
分析 A、稀有气体分子晶体中不存在任何化学键;
B、离子晶体指的是阴阳离子通过离子键结合形成的晶体;
C、含有极性键的分子不一定是极性分子;
D、含有非极性键的分子不一定是非极性分子,如过氧化氢分子.
解答 解:A、分子晶体中可能不含共价键,如稀有气体,故A错误;
B、离子晶体指的是阴阳离子通过离子键结合形成的晶体,故离子晶体中一定含有离子键,故B正确;
C、含有极性键的分子不一定是极性分子,如果分子正负电荷重心重合,则就是非极性分子,如CCl4,故C错误;
D、含有非极性键的分子不一定是非极性分子,如过氧化氢分子,故D错误;
故选B.
点评 本题考查了化学键和物质的关系,注意不是所有的物质都含有化学键,如稀有气体分子中不含化学键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
| 实 验 现 象 | 可 以 肯 定 的 结 论 |
| A、观察混合气体无色 | 无Cl2、 |
| B、将混合气体通过浓H2SO4,体积减小 | 有NH3、无HCl |
| C、剩余气体跟空气接触后变为红棕色 | 有NO、无O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
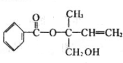
| A. | 有机物X的含氧官能团有3种 | |
| B. | X分子中苯环上的一氯取代物有3种 | |
| C. | 在Ni作催化剂的条件下,1mol X 最多能与5 mol H2加成 | |
| D. | X在一定条件下能发生加成、取代、消去等反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当通入的Cl2为2.24 L时,反应中电子转移数目为0.1 NA | |
| B. | 当溶液中Na+为0.4 NA时,溶液中的Cl-为0.2 NA | |
| C. | 当电子转移数目为0.2 NA时,溶液质量增加14.2 g | |
| D. | 当溶液质量增加7.1 g时,溶液中ClO-为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
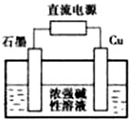 金属单质及其化合物在工农业生产中应用广泛.
金属单质及其化合物在工农业生产中应用广泛.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 采用“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”可提高空气质量 | |
| B. | 酸性氧化物均能与水反应生成对应的酸,如CO2、SiO2、SO3 | |
| C. | 石油化工中的裂化、裂解过程都是通过化学反应来获得气态烯烃 | |
| D. | 乙醇、过氧化氢、次氯酸钠等均通过氧化作用达到杀菌消毒的目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
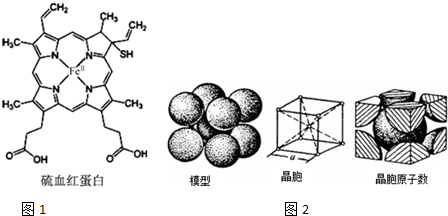
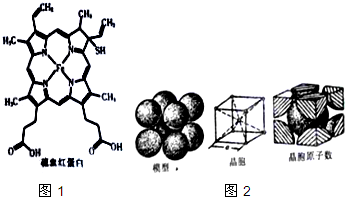 血红蛋白是高等生物体内负责运载氧的一种蛋白质(缩写为HB或HCB).与正常血红蛋白相比,硫血红蛋白不能与氧结合,因此失去携带氧的能力.如图1所示为硫血红蛋白的结构.请回答下列问题:
血红蛋白是高等生物体内负责运载氧的一种蛋白质(缩写为HB或HCB).与正常血红蛋白相比,硫血红蛋白不能与氧结合,因此失去携带氧的能力.如图1所示为硫血红蛋白的结构.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com