
下列关于燃烧热的说法中正确的是()
A. 1 mol物质燃烧所放出的热量
B. 常温下,可燃物燃烧放出的热量
C. 在25℃、1.01×105Pa时,1mol纯物质燃烧生成稳定的氧化物时所放出的热量
D. 燃烧热随化学方程式前的化学计量数的改变而改变
考点: 燃烧热.
专题: 化学反应中的能量变化.
分析: 燃烧热的条件是在25℃、1.01×105Pa下,必须是1mol物质完全燃烧并且生成的物质为最稳当的氧化物,燃烧热的热化学方式的计量系数必须是1,据此解答.
解答: 解:A.燃烧热必须是可燃物质完全燃烧生成稳定的氧化物放出的热量,故A错误;
B.可燃物燃烧可以是完全燃烧也可以是不完全燃烧,而燃烧热必须是全燃烧放出的热量,故B错误;
C.在25℃、1.01×105Pa时,1mol纯物质燃烧生成稳定的氧化物时所放出的热量,故C正确;
D.燃烧热化学方程式前的化学计量数必须是1,故D错误;
故选:C.
点评: 本题考查了燃烧热的定义,属于对课本基本知识的考查,难度不大,理解燃烧热的概念是解题的关键.


科目:高中化学 来源: 题型:
制备氯化物时,常用两种方法:①用金属与氯气直接化合制得;②用金属与盐酸反应制得.用以上两种方法都可制得的氯化物是()
A. AlCl3 B. FeCl3 C. FeCl2 D. CuCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,某密闭容器中发生反应:N2(g)+3H2(g)═2NH3(g).反应物N2的浓度10s内从2mol/L降为1mol/L,在这段时间内用N2浓度的变化表示的反应速率为( )
A. 0.05 mol/(L•s) B. 0.1 mol/(L•s) C. 0.15 mol/(L•s) D. 0.2 mol/(L•s)
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素的一个原子形成的离子可表示为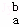 Xn﹣,下列说法正确的是( )
Xn﹣,下列说法正确的是( )
A. 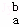 Xn﹣含有的中子数为a+b
Xn﹣含有的中子数为a+b
B. 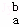 Xn﹣含有的电子数为a﹣n
Xn﹣含有的电子数为a﹣n
C. X原子的质量数为a+b+n
D. 一个X原子的质量约为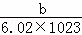 g
g
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:
①元素周期表中,Z与Y相邻,Z与W也相邻;
②Y、Z和W三种元素的原子最外层电子数之和为17.
请填空:
(1)Y、Z和W三种元素是否位于同一周期(填“是”或“否”): ,理由是
(2)Y是 ,Z是 ,W是 ;
(3)X、Y、Z和W可组成一化合物,其原子个数之比为8:2:4:1.写出该化合物的名称及化学式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是()
A. 增大压强,活化分子数增加,化学反应速率一定增大
B. 升高温度,活化分子百分数增加,化学反应速率一定增大
C. 活化分子间所发生的分子间的碰撞为有效碰撞
D. 加入反应物,使活化分子百分数增加,化学反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
已知充分燃烧a g乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是()
A. 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l);△H=﹣4b kJ/mol
B. C2H2(g)+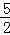 O2(g)═2CO2(g)+H2O(l);△H=2b kJ/mol
O2(g)═2CO2(g)+H2O(l);△H=2b kJ/mol
C. 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l);△H=2b kJ/mol
D. 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l);△H=b kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
依据事实,写出下列反应的热化学方程式.
(1)1molN2(g)与适量O2(g)反应生成NO2(g),吸收68kJ热量: ;
(2)1molCu(s)与适量O2(g)反应生成CuO(s),放出157kJ热量: ;
(3)卫星发射时可用肼(N2H4)作燃料,1mol N2H4(l)在O2(g)中燃烧,生成N2(g)和H2O(l),放出622kJ热量:
(4)10g C2H6(g)完全燃烧生成CO2(g)和H2O(l),放出a kJ热量,写出表示C2H6燃烧热的热化学方程式:
(5)已知:WO2(s)+2H2(g)═W(s)+2H2O(g)△H=+66.0kJ/mol;WO2(g)+2H2(g)═W(s)+2H2O(g)△H=﹣137.9kJ/mol.则WO2(s)═WO2(g)的△H=
(6)已知:Al2O3(s)+AlCl3(g)+3C(s)═3AlCl(g)+3CO(g)△H=a kJ/mol,2Al(l)+AlCl3(g)═3AlCl(g)△H=b kJ/mol,则反应Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H= J/mol(用含a、b的代数式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
各可逆反应达平衡后,改变反应条件,其变化趋势正确的是( )
|
| A. |
FeCl3+3KSCN⇌Fe(SCN)3+KCl(忽略液体体积变化) |
|
| B. |
2NO+O2⇌2NO2△H<0 |
|
| C. |
NO(g)+CO(g)⇌ |
|
| D. |
A2(g)+3B2(g)⇌2AB3(g)△H=﹣373.4KJ•mol﹣1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com