
| A. | ①③ | B. | ②③⑤ | C. | ④⑥ | D. | ①②⑤ |
分析 弱电解质在溶液中部分电离,存在电离平衡,要说明HF是弱电解质,只要能证明HF部分电离即可,注意酸的溶解性及酸的通性无法确定酸电离的程度,据此进行解答.
解答 解:①常温下碱性溶液中pH>7,NaF溶液的pH大于7说明呈碱性,说明NaF发生了水解,HF是弱酸,故①正确;
②导电性强弱主要与离子浓度有关,不能说明HF是弱酸,故②错误;
③常温下0.1mol/L的HF溶液的pH为2.3说明HF部分电离是弱酸,故③正确;
④HF能与Na2CO3溶液反应,产生CO2气体说明HF的酸性比碳酸的强,不能说明HF是弱酸,故④错误;
⑤HF与水能以任意比混溶,属于氟化氢的物理性质,与HF的酸性强弱无关,故⑤错误;
⑥1mol/L的HF水溶液能使紫色石蕊试液变红说明HF水溶液显酸性,不能说明HF是弱酸,故⑥错误;
故选A.
点评 本题考查了弱电解质的判断,题目难度不大,熟练掌握弱电解质的特征“部分电离”是解答本题的关键,试题侧重基础知识的考查,有利于提高学生的灵活应用能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 烃类分子中的碳原子与其他原子间通过非极性键结合 | |
| B. | 烷烃是饱和的链烃,分子中碳原子不可能在同一平面上 | |
| C. | 甲烷中混有乙烯,将其通入酸性高锰酸钾溶液中洗气 | |
| D. | 烷烃的沸点随碳原子数增加而逐渐升高 |
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上第二次月考化学试卷(解析版) 题型:填空题
I:氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成它。CuH不稳定、易分解、在氯气中能燃烧,与稀盐酸反应能生成气体;Cu+在酸性条件下发生的反应是2Cu+= Cu2++Cu。根据以上信息回答:
(1)用CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中所起的作用是____________。
(2)写出CuH在氯气中燃烧的化学反应方程式________________________。
(3)CuH溶解在稀盐酸中生成的气体是______________,如果反应中生成了标准状况下22.4 L的气体,被还原的离子得电子的物质的量是__________。
II:用高效的二氧化氯(ClO2)替代液氯进行消毒,可避免产生对人体健康有害的有机氯代物。
(1)工业上,ClO2常用NaClO3和Na2SO3溶液混合并加硫酸酸化后反应制得,则化学反应方程式为__________________________。
(2) 有效氯含量是含氯消毒剂的一个重要指标,有效氯含量的定义:从HI中氧化出相同量的I2所需Cl2的质量与指定含氯消毒剂的质量之比,常用百分数表示。则ClO2的有效氯含量是___________。
(3)某同学欲对用ClO2消毒过的自来水进行氯元素含量的测定(假定ClO2全部转化为Cl-),他进行了如下实验:向30.00 mL水样中加几滴K2CrO4溶液作指示剂,用0.001 mol·L-1 AgNO3溶液滴定,当有砖红色Ag2CrO4沉淀出现时,达滴定终点,此时用去AgNO3溶液12.12 mL。
①水样中Cl-的物质的量浓度是__________。
②已知Ksp(AgCl)=1.78×10-10,Ksp(Ag2CrO4)=2.00×10-12。如在滴定终点时,测得溶液中CrO42-的浓度是5.0×10-3mol·L-1。试计算此时溶液中Cl-的浓度是_________。
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上第二次模拟化学试卷(解析版) 题型:推断题
咖啡酸苯乙酯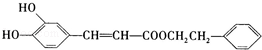 是一种天然抗癌药物,在一定条件下能发生如下转化:
是一种天然抗癌药物,在一定条件下能发生如下转化:
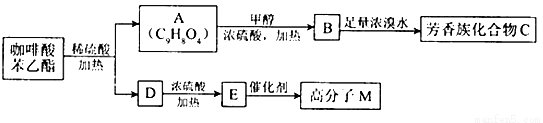
请填写下列空白.
(1)D分子中的官能团是______________;高分子M的结构简式是______________.
(2)写出A→B反应的化学方程式:______________.
(3)B→C发生的反应类型有______________.
(4)A的同分异构体很多种,其中,同时符合下列条件的同分异构体有_________种.
①苯环上只有两个取代基;
②能发生银镜反应;
③能与碳酸氢钠溶液反应;
④能与氯化铁溶液发生显色反应.
(5)以下对A具有的性质描述正确的是__________
a.1molA可消耗2molNaOH
b.一定 条件下1molA最多能与1mol氢气加成
条件下1molA最多能与1mol氢气加成
c.能发生银镜反应
d.能发生取代反应.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去96%的乙醇中的少量水制无水乙醇:加入生石灰,振荡、静置、蒸馏 | |
| B. | 除去溴苯中混有的少量单质溴:加入足量的NaOH溶液,振荡、静置、分液 | |
| C. | CH4和CCl4中的化学键均为非极性键,CH4、CCl4都是正四面体结构 | |
| D. | 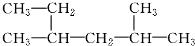 系统命名法为:2,4-二甲基-己烷 系统命名法为:2,4-二甲基-己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2+Ca(OH)2=CaCO3↓+H2O | B. | SO3+H2O=H2SO4 | ||
| C. | 2KMnO4=K2MnO4+MnO2+O2↑ | D. | 2NaHCO3=Na2CO3+CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
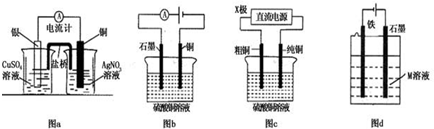
| A. | 图a是原电池装置,且较长时间内,电流计会显示有稳定电流产生 | |
| B. | 图b 电解足量硫酸铜溶液一段时间后,加入适量CuCO3固体,可以使硫酸铜溶液恢复到原浓度 | |
| C. | 图c中的X极若为负极,则该装置可实现粗铜的精炼 | |
| D. | 图d中若M是海水,该装置是通过“牺牲阳极保护法”使铁不被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大理石和盐酸的反应:CO32ˉ+2H+═CO2↑+H2O | |
| B. | KI溶液中加入硫酸酸化的过氧化氢溶液:2I-+H2O2═I2+2OH- | |
| C. | 三氯化铁溶液与铁反应:Fe3++Fe═2Fe2+ | |
| D. | 二氧化硅与氢氧化钠溶液反应:SiO2+2OHˉ═SiO32ˉ+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 我们常用的元素周期表中元素排序的依据是元素的相对原子质量 | |
| B. | 元素周期表中同一横行元素原子的电子层数相同 | |
| C. | 元素周期表有16个纵行 | |
| D. | 元素周期表已发展成一个稳定的形式,它不可能再有新的变化了 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com