
���� ��1���Ȼ���������Ϊ0.287g���������ʵ���Ϊ��$\frac{0.287g}{143.5g/mol}$=0.002mol���������������ʵ���Ϊ$\frac{0.002mol}{2}$=0.001mol�������µ����Ϊ0.0224L��
��2����Ӧ�����Ȼ��ƺʹ������ƣ��������غ�n��NaOH��=2n��Cl2���������
��3��Cl2���������ɵ�I2������ⱻ����ΪIO3-�����Է�Ӧ����ʽΪ��3H2O+5Cl2+5I-=2I2+IO3-+10Cl-+6H+��
��� �⣺��1���Ȼ���������Ϊ0.287g���������ʵ���Ϊ��$\frac{0.287g}{143.5g/mol}$=0.002mol���������������ʵ���Ϊ$\frac{0.002mol}{2}$=0.001mol�������µ����Ϊ0.0224L�����Ը÷�����Ʒ��Cl2���������Ϊ$\frac{0.0224L}{1.00L}��100%$=2.24%���ʴ�Ϊ��2.24%��
��2��n��NaOH��=0.001mol��2=0.02 mol������NaOH��Һ�����ʵ���Ũ��Ϊ0.02 mol/L���ʴ�Ϊ��0.02 mol/L��
��3��Cl2���������ɵ�I2������ⱻ����ΪIO3-�����Է�Ӧ����ʽΪ��3H2O+5Cl2+5I-=2I2+IO3-+10Cl-+6H+�������ɵ�I2��IO3-�����ʵ���֮��Ϊ2��1���ʴ�Ϊ��2��1��
���� ���⿼����������ԭ��Ӧ�͵����ӷ���ʽ��д����Ŀ�Ѷ��еȣ���ȷ��Ӧ�����������������Ӱ��Ϊ���ؼ���ע���������ӷ���ʽ����дԭ��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
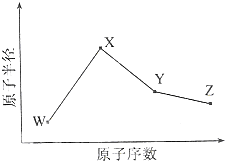 W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯��ͼ��ʾ����֪W��һ�ֺ��ص�������Ϊ18��������Ϊ10��X��Neԭ�ӵĺ�����������1��Y�ĵ�����һ�ֳ����İ뵼����ϣ�Z�ĵ縺����ͬ��������Ԫ�������
W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯��ͼ��ʾ����֪W��һ�ֺ��ص�������Ϊ18��������Ϊ10��X��Neԭ�ӵĺ�����������1��Y�ĵ�����һ�ֳ����İ뵼����ϣ�Z�ĵ縺����ͬ��������Ԫ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ax/100bmol/L | B�� | ax/500bmol/L | C�� | ax/2000bmol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ���³�ѹ�£�1.7gH2O2�к��еĵ�����Ϊ0.9nA | |
| B�� | 1L1 mol��L-1CuCl2��Һ����2nA��Cl- | |
| C�� | 1 mol Na ������ O2��Ӧ������Na2O��Na2O2�Ļ�����ʧȥ2nA������ | |
| D�� | ��״���£�2.24L��������������Ϊ0.1nA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
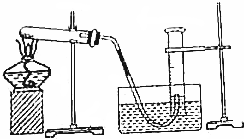
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
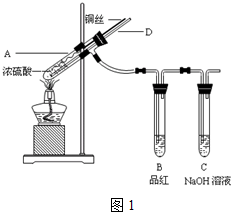

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2 H2O2$\frac{\underline{\;����\;}}{\;}$2 H2O+O2�� | B�� | 2 Al��OH��3$\frac{\underline{\;\;��\;\;}}{\;}$Al2O3+3 H2O | ||
| C�� | Fe2O3+3 CO$\frac{\underline{\;����\;}}{\;}$2 Fe+3 CO2 | D�� | Cl2+H2O�THCl+HclO |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com