
| A. | 0.1L | B. | 0.2L | C. | 0.4L | D. | 0.5L |
分析 FeO、Fe3O4的混合物,在足量H2气流中加热充分反应,冷却后称得剩余固体比原混合物减轻0.8g为混合物中氧原子的质量;将等质量的FeO、Fe3O4的混合物与硫酸反应,欲使之完全溶解,当恰好反应时需要硫酸的体积最小,此时恰好生成FeSO4、Fe2(SO4)3,SO42-与FeO、Fe3O4 的混合物中O原子物质的量相等.
解答 解:FeO、Fe3O4的混合物,在足量H2气流中加热充分反应,冷却后称得剩余固体比原混合物减轻0.8g为混合物中氧原子的质量,其物质的量$\frac{0.8g}{16g/mol}$=0.05mol;
将等质量的FeO、Fe3O4的混合物与硫酸反应,欲使之完全溶解,当恰好反应时需要硫酸的体积最小,此时恰好生成FeSO4、Fe2(SO4)3,SO42-与FeO、Fe3O4 的混合物中O原子物质的量相等,故n(H2SO4)=0.05mol,需0.5mol•L-1的硫酸的体积至少为$\frac{0.05mol}{0.5mol/L}$=0.1L,
故选:A.
点评 本题考查混合物的计算,难度中等,关键是判断混合物中O原子与硫酸根的数量关系,避免利用过程法的繁琐.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
A、利用该装置准确量取9.20ml硫酸溶液 | B、将洗涤液转移到容量瓶中,应该采取如图的操作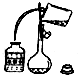 |
| C、过滤和蒸发中都需要使用玻璃棒,且玻璃棒的用途一样 | D、保存NaOH应使用带橡皮塞的玻璃试剂瓶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| H2(g) | Cl2 (g) | HCl (g) | |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | 243 | a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中,K+、Ca2+、Cl2、Br-可以大量共存 | |
| B. | 能使含I2的淀粉溶液蓝色褪去,说明NaHSO3溶液具漂白性 | |
| C. | 与FeCl3反应的离子方程式:SO32-+2Fe3++H2O=SO42-+2Fe2++2H+ | |
| D. | 和足量Ca(OH)2溶液反应的离子方程式:Ca2++OH-+HSO3-=CaSO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的标准燃烧热为-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| B. | 500℃、30MPa下,将0.5molN2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) $?_{500℉、30MPa}^{催化剂}$2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | 氯化镁溶液与氨水反应:Mg2++2OH-═Mg(OH)2↓ | |
| D. | CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)═2CO(g)+O2(g)反应△H=+2×283.0 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com