
| A. | 硅 | B. | 氨气 | C. | 醋酸 | D. | 氢氧化钡 |
分析 电解质是指在水溶液或熔化状态下都能导电的化合物;强电解质在水溶液或熔融状态下,能完全电离成离子的电解质;弱电解质为:在水溶液里部分电离的电解质,包括弱酸、弱碱、水与少数盐,据此即可解答.
解答 解:A、硅为单质,既不是电解质也不是非电解质,故A错误;
B、氨气在水溶液中和熔融状态下均不能电离出离子而导电,故为非电解质,故B错误;
C、醋酸在溶液中不能完全电离,故为弱电解质,故C正确;
D、氢氧化钡在水溶液中能完全电离,故为强电解质,故D错误.
故选C.
点评 本题考查了强弱电解质的判断,题目难度不大,注意明确强电解质与弱电解质的本质区别为能否完全电离,试题有利于培养学生灵活应用所学知识解决实际问题能力.


科目:高中化学 来源: 题型:选择题
| A. | 若二氧化碳气体中混有少量的一氧化碳气体,可用点燃的方法除去 | |
| B. | 将铜粉中混有的少量铁粉除去,加入过量的CuSO4溶液充分反应后,过滤、洗涤干燥 | |
| C. | 将KNO3固体中混有的少量NaCl固体除去,可以用冷却KNO3的热饱和溶液、过滤即可 | |
| D. | 若氧气中混有少量的二氧化碳气体,可将混合气体通过足量的NaOH溶液后干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯、乙醇、四氯化碳都是重要有机溶剂,都可用于提取碘水中的碘单质 | |
| B. | 在强碱性溶液中,[Al(OH)4]-、HCO3-、Na+、Ca2+可能同时大量共存 | |
| C. | 铁船底镶嵌锌块,构成原电池,锌作负极,以防船体被腐蚀 | |
| D. | 用量筒量取10.mL 1.0mol/L的盐酸于100mL溶液瓶中,加水稀释至刻度,可制得0.1mol/L的盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下pH=13的溶液中:NH4+、Na+、Cl-、CO32- | |
| B. | 能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、NH4+ | |
| C. | 能够与金属Cu常温下反应放出气体的溶液:Na+、Al3+、SO42-、K+ | |
| D. | 漂白粉的水溶液中:Fe2+、Cl-、Ca2+、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某物质的溶液中由水电离出的c(H+)=1×10-amol/L,若a>7时,则该溶液的pH一定为14-a | |
| B. | 相同物质的量浓度的下列溶液中,①NH4Al(SO4)2、②(NH4)2SO4、③CH3COONH4、④NH3•H2O;c(NH4+)由大到小的顺序是:②>①>③>④ | |
| C. | 物质的量浓度相等的 H2S 和 NaHS 混合溶液中:c(Na+)+c(H+)=c(S2-)+c (HS-)+c(OH-) | |
| D. | AgCl悬浊液中存在平衡:AgCl(s)?Ag+(aq)+Cl-(aq),往其中加入少量 NaCl粉末,平衡会向左移动,Ksp减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100 g质量分数为98%的浓硫酸中所含有的氧原子数为4 NA | |
| B. | 足量的Fe与6.72 L Cl2反应转移的电子数为0.6 NA | |
| C. | 密闭容器中1 molN2与4 molH2反应生成的NH3分子数小于2NA | |
| D. | 3 g乙烷含有共用电子对为0.6 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、Na+、Cl-、SiO32- | B. | Fe3+、Ba2+、I-、NO3- | ||
| C. | NH4+、K+、S2-、SO32- | D. | H+、Ca2+、F-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
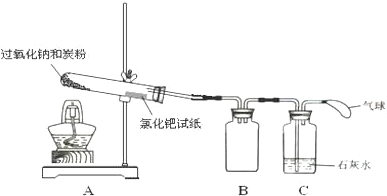
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当$\frac{a}{b}$>2时,发生的离子反应为:CO32-+H+═HCO3-,HCO3-+H+═CO2↑+H2O | |
| B. | 当0<$\frac{a}{b}$<1时,发生的离子反应为:CO32-+H+═HCO3- | |
| C. | 当2a=3b时,发生的离子反应为:2CO32-+3H+═HCO3-+CO2↑+H2O | |
| D. | 当1<$\frac{a}{b}$<2时,溶液中n(HCO3-)为(2a-b)mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com