
【题目】若1.8g 某金属与足量的盐酸反应后,产生的H2在标准状况下体积为2.24L,则该金属为
A. Al B. Mg C. Fe D. Zn
【答案】A
【解析】设金属在化合物中的化合价为x,金属的摩尔质量为M,
酸足量时生成的标准状况下的氢气体积为2.24L,则其物质的量为![]() =0.1mol,由电子守恒可知,
=0.1mol,由电子守恒可知, ![]() ×(x-0)=0.1mol×2×(1-0),即9x=M;A.铝的摩尔质量为27g/mol,在化合物中的化合价为+3价,符合9x=M,故A正确;B.镁的摩尔质量为24g/mol,在化合物中的化合价为+2价,不符合9x=M,故B错误;C.铁的摩尔质量为56g/mol,与盐酸反应后生成的化合物中的化合价为+2价,不符合9x=M,故C错误;D.锌的摩尔质量为65g/mol,在化合物中的化合价为+2价,不符合9x=M,故D错误;故选A。
×(x-0)=0.1mol×2×(1-0),即9x=M;A.铝的摩尔质量为27g/mol,在化合物中的化合价为+3价,符合9x=M,故A正确;B.镁的摩尔质量为24g/mol,在化合物中的化合价为+2价,不符合9x=M,故B错误;C.铁的摩尔质量为56g/mol,与盐酸反应后生成的化合物中的化合价为+2价,不符合9x=M,故C错误;D.锌的摩尔质量为65g/mol,在化合物中的化合价为+2价,不符合9x=M,故D错误;故选A。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】将1.12 g铁粉加到25 mL 2 mol/L的氯化铁溶液中,完全反应后,其结果是
A. 铁有剩余,溶液呈浅绿色,c(Cl-)基本不变
B. 往溶液中滴加无色KSCN溶液,未显红色
C. 溶液中n(Fe2+)与n(Fe3+)之比为6∶1
D. 氧化产物与还原产物的物质的量之比为2∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往盛氯水的试管里滴入少量紫色石蕊试液,观察到的现象是 ( )
A. 紫色石蕊试液显蓝色
B. 紫色石蕊试液显红色
C. 紫色石蕊试液的颜色消失
D. 紫色石蕊试液先显红色,后红色消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁被称为“国防金属”,镁及其合金用途很广,目前世界上60%的镁从海水中提取。从海水中提取镁的流程如下:
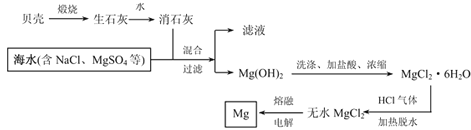
请根据上述流程图和镁及化合物的性质回答下列问题:
(1)用贝壳煅烧生石灰的反应方程式:________________
(2)氢氧化镁溶于盐酸的离子方程式为:_____________。
(3)简述,由MgCl2·6H2O制无水MgCl2,加热时通HCl气体的主要原因是:___________。
(4)金属镁属于(填写下列编号):___________。
a.黑色金属 b.有色金属 c.轻金属 d.重金属 e.贵金属
(5)Mg(OH)2煅烧可得熔点很高的MgO,MgO的电子式为:____________。
(6)MgCl2和AlCl3的熔点均较低,加MgO和Al2O3的熔点都很高。为什么冶炼金属镁是电解MgCl2,而冶炼金属铝则电解Al2O3:_______________。
(7)某MgCl2溶液的浓度为0.01mol/L,在该溶液中滴加NaOH溶液至pH=10,此时溶液中的Mg2+是否沉淀完全?_________(填“是”或“否”),此时c(Mg2+)=_________。
(已知:Ksp[Mg(OH)2]=1.8×10-11)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组为探究元素周期表中元素性质的递变规律,设计了如下实验。
Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:________与盐酸反应最剧烈,________与盐酸反应的速度最慢;________与盐酸反应产生的气体最多。
向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为_______________。
(3)资料显示:钠、镁、铝都可以用于制备储氢的金属氢化物。
① NaH是离子化合物,能与水发生氧化还原反应生成H2,该反应的还原剂是________________。
② NaAlH4是一种良好的储氢材料。NaAlH4与水反应产生氢气的化学方程式为____________________。
Ⅱ.为验证氯、溴、碘三种元素的非金属性强弱,用下图所示装置进行试验(夹持仪器已略去,气密性已检验)。

实验过程:
①打开弹簧夹,打开活塞a,滴加浓盐酸。
②当B和C中的溶液都变为黄色时,夹紧弹簧夹。
③当B中溶液由黄色变为棕红色时,关闭活塞a。
④……
(1)A中发生反应生成氯气,请写出该反应的离子方程式:___________________。
(2)验证氯气的氧化性强于碘的实验现象是________________________。
(3)B、C管口“浸有NaOH溶液的棉花”的作用是__________________________。
(4)为验证溴的氧化性强于碘,过程④的操作和现象是______________________。
(5)过程③实验的目的是____________________。
(6)请运用原子结构理论解释氯、溴、碘非金属性逐渐减弱的原因:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化合物在一定条件下,既能发生消去反应,又能发生水解反应的是( )
A.CH3Cl B.CH3CH(Br)CH3 C.(CH3)3C—CH2Cl D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学键的说法正确的是( )
A. 相邻的两个原子间可以形成化学键,多个原子间不可能形成化学键
B. 化合物中一定含有化学键,单质中也一定含有化学键
C. 相邻的两个或多个原子间的相互作用一定是化学键
D. 阴、阳离子之间的强相互作用也是化学键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com