
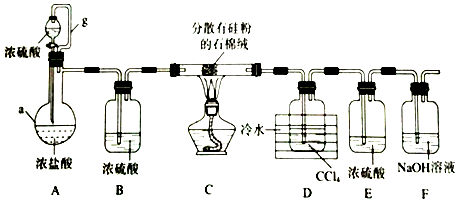
分析 粗硅提纯:装置A,蒸馏烧瓶中盛放浓盐酸,分液漏斗中盛放浓硫酸,利用浓硫酸的吸水性以及氯化氢的挥发性,打开分液漏斗活塞,从A中排出氯化氢气体,排尽装置中的空气,装置B,对氯化氢气体进行干燥,装置C,粗硅与干燥HCl气体反应制得SiHCl3:Si+3HCl$\frac{\underline{\;\;△\;\;}}{\;}$SiHCl3+H2;装置F中的氢氧化钠是为了吸收过量的氯化氢,装置E防止F中的水蒸气进入装置D与SiHCl3发生反应,装置D收集SiHCl3,通过装置F后,剩余气体为氢气,可通过点燃或气囊收集处理.
(1)根据仪器a的特征以及常见仪器的名称解答,装置A中的b导管是为了平衡压强的作用;
(2)浓硫酸具有吸水性,氯化氢易挥发,SiHCl3能与水剧烈反应,在空气中易被氧化;
(3)硅和氯化氢在加热的条件下反应生成和三氯硅烷和氢气;
(4)得到的产物沸点不同,可以控制沸点通过蒸馏的方法得到SiHCl3;
(5)反应后的气体为氢气,氢气具有可可燃性,可通过燃烧或气囊收集的方法处理尾气;
(6)SiHCl3在潮湿的空气中被氧化,生成一种氧化物为二氧化硅,一种无氧酸根据原子守恒可知为氯化氢.
解答 解:(1)仪器a是具有支管的烧瓶,为蒸馏烧瓶,装置A中的b导管是为了平衡压强的作用,使分液漏斗中的液体浓硫酸顺利流下,
故答案为:蒸馏烧瓶;平衡压强,使浓硫酸容易滴加(或其它合理答案);
(2)装置A,蒸馏烧瓶中盛放浓盐酸,分液漏斗中盛放浓硫酸,利用浓硫酸的吸水性以及氯化氢的挥发性,打开分液漏斗活塞,从A中排出氯化氢气体,SiHCl3的沸点为33.0°C,易溶于有机溶剂,能与水剧烈反应,在空气中易被氧化,实验时,需先打开分液漏斗活塞,一段时间后,在点燃C处酒精灯,排尽装置中的空气,避免SiHCl3与空气中的水蒸气反应和被O2氧化,
故答案为:吸水性; 排尽装置中的空气,避免SiHCl3与空气中的水蒸气反应和被O2氧化;
(3)根据题干信息,硅单质和HCl反应生成SiHCl3可知,硅和氯化氢反应的方程式为:Si+3HCl$\frac{\underline{\;\;△\;\;}}{\;}$SiHCl3+H2,
故答案为:Si+3HCl$\frac{\underline{\;\;△\;\;}}{\;}$SiHCl3+H2;
(4)SiHCl3的沸点为33.0°C,易溶于有机溶剂,制出的SiHCl3可能不纯,提纯SiHCl3的方法是利用其沸点较低,通过蒸馏的方法分离得到纯净的SiHCl3,
故答案为:蒸馏;
(5)硅单质和HCl反应Si+3HCl$\frac{\underline{\;\;△\;\;}}{\;}$SiHCl3+H2,粗硅与干燥HCl气体反应制得SiHCl3:Si+3HCl$\frac{\underline{\;\;△\;\;}}{\;}$SiHCl3+H2;装置F中的氢氧化钠是为了吸收过量的氯化氢,通过装置F后,剩余气体为氢气,氢气燃烧生成水,可通过点燃或气囊收集处理,
故答案为:点燃(或气囊收集);
(6)硅的稳定氧化物为二氧化硅,SiHCl3在潮湿的空气中被氧化,生成一种氧化物为二氧化硅,根据原子守恒可知一种无氧酸为氯化氢,所以该反应的化学方程式为:2SiHCl3+O2+2H2O═2SiO2+6HCl,
故答案为:2SiHCl3+O2+2H2O═2SiO2+6HCl.
点评 本题考查了粗硅的提纯,题目难度中等,明确实验原理和实验目的是解题关键,注意硅及其化合物的性质,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9m~10-7m之间 | |
| B. | 用平行光照射NaCl溶液和Fe(OH)3胶体,可以加以区分 | |
| C. | 把FeCl3饱和溶液与NaOH溶液混合,以制取Fe(OH)3胶体 | |
| D. | 除去Fe(OH)3胶体中的H+、Cl-,可用渗析的实验方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2v正(B)=v逆(C) | B. | 该体系的密度都不随时间变化 | ||
| C. | 1molA断裂,同时1molC也断裂 | D. | 该体系的温度不随时间而变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. |  =KCl+3Cl2↑+3H2O =KCl+3Cl2↑+3H2O | |
| B. | H2S+H2SO4(浓)═S↓+SO2↑+2H2O | |
| C. | 2H2S+SO2═3S↓+2H2O中氧化剂与还原剂的物质的量之比是1:2 | |
| D. | 3NO2+H2O═2HNO3+NO中氧化剂与还原剂的物质的量之比是1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com