
【题目】铝土矿的主要成分是Al2O3、SiO2和Fe2O3等。从铝土矿中提炼Al2O3的流程

下列说法中错误的是
A. 滤液Ⅰ的主要成分是Na2SiO3、NaAlO2和NaOH
B. 滤液Ⅲ的含大量的阴离子是HCO3-
C. 反应Y的离子方程式是2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
D. 滤液Ⅱ中通入过量的X的目的是使AlO2-充分沉淀而不引进杂质
【答案】C
【解析】根据铝土矿的成分,Fe2O3属于碱性氧化物,不与NaOH反应,Al2O3属于两性氧化物,与NaOH反应生成NaAlO2,SiO2属于酸性氧化物,与NaOH反应生成Na2SiO3,因此滤液I中的成分是Na2SiO3、NaAlO2以及过量NaOH,故说法正确;B、加入CaO后,CaO与水反应生成Ca(OH)2,Ca(OH)2+Na2SiO3=CaSiO3↓+2NaOH,滤液Ⅱ中含有NaAlO2,通入足量的CO2,发生AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,故说法正确;C、因为通入足量的CO2,生成的HCO3-,故说法错误;D、碳酸的酸性强于氢氧化铝,通入足量的CO2,产生氢氧化铝沉淀,不引入新杂质,故说法正确。


科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是

A. 通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大
B. 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C. 负极反应为2H2O 4e– = O2+4H+,负极区溶液pH降低
D. 当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2C2O4为二元弱酸。20℃配制一组c(H2C2O4)+c(HC2O4–)+c(C2O42–)=0.100 mol·L–1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。一定正确的是
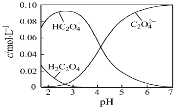
A.pH=2.5的溶液中:c(H2C2O4)+c(C2O42–)>c(HC2O4–)
B.c(Na+)=0.100 mol·L–1的溶液中:c(H+)+c(H2C2O4)=c(OH–)+c(C2O42–)
C.c(HC2O4–)=c(C2O42–)的溶液中:c(Na+)>0.100 mol·L–1+c(HC2O4–)
D.pH=7的溶液中:c(Na+)<2c(C2O42–)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电池与现代人的生活密切相关,某同学为了研究原电池原理设计了如图所示的装置。下列说法错误的是

A. X、Y不用导线连接时,铜棒上会有银析出
B. X和Y用导线连接时,银棒上发生的电极反应为Ag++e-==Ag
C. X和Y用导线连接时,电子由银经导线移向铜,再经电解质溶液移向银
D. 无论X和Y是否用导线连接,铜棒均会溶解,溶液都从无色逐渐变成蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F可用于制造香精,可利用下列路线合成。

回答下列问题:
(1)![]() 分子中可能共面的原子最多有_____个;
分子中可能共面的原子最多有_____个;
(2)物质A的名称是______;
(3)物质D中含氧官能团的名称是_______;
(4)“反应④”的反应类型是______;
(5)写出“反应⑥”的化学方程式:________;
(6)C有多种同分异构体,与C中所含有的官能团相同的有_____种,其中核磁共振氢谱为四组峰的结构简式为 和_______。
和_______。
(7)参照上述合成路线,以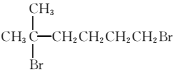 为原料(无机试剂任选),设计制备
为原料(无机试剂任选),设计制备![]() 的合成路线:_______________。
的合成路线:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】摩尔盐易[(NH4)2Fe(SO4)2]易溶于水,具有还原性。以下是利用废铁屑、稀硫酸和硫酸铵为原料制取摩尔盐的流程图。

回答下列问题:
(1)在“步骤l”中加Na2CO3溶液是为了洗涤除去废铁屑表面的油污,加热的目的是______(利用简要文字和必要的离子方程式说明),配制100g10%的Na2CO3溶液需要的仪器有药匙、量筒、烧杯、玻璃棒和_______;
(2)“步骤2”中所用废铁屑必须过量,原因是______________;
(3)“步骤3”加入(NH4)2SO4固体充分搅拌溶解后,依次进行的实验操作是:蒸发浓缩、______、过滤、洗涤、干燥;
(4)一般采用滴定法测定摩尔盐产品中Fe2+的含量:称取4.0g摩尔盐样品,溶于水,加入适量稀硫酸,用0.2 mol/LKMnO4溶液滴定,达到终点时,消耗10.00 mL KMnO4溶液。
① 滴定过程中发生反应的离子方程式为___________;
② 产品中Fe2+的质量分数为_________;
③ 滴定过程中.左手控制________,右手摇动锥形瓶,直到_________时停止滴定,读数。此时若俯视读数.测定结果将偏________(填“高”或“低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知醋酸达到电离平衡后,改变某条件电离平衡向正反应方向移动,则下列说法正确的是( )
A. 实现该变化的只能是升高温度
B. 溶液的导电能力一定变强
C. 溶液的pH一定减小
D. 发生电离的分子总数增多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C5H7Br 的有机物,不可能是
A. 只含有1个双键的直链有机物 B. 含有2个双键的直链有机物
C. 含有1个双键的环状有机物 D. 含有1个叁键的直链有机物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com