


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案科目:高中化学 来源: 题型:
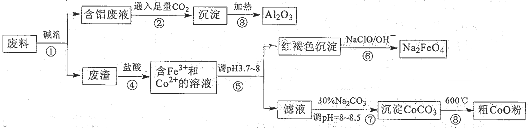
| 温度/℃ | 32 | 52 | 90 | 120 |
| 固体质量/g | ① | 83 | 74 | 65 |
| 固体物质化学式 | CoCl2?6H2O | ② | ③ | CoCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
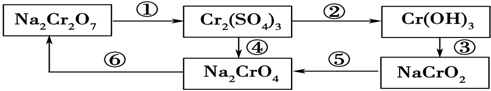
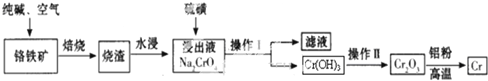
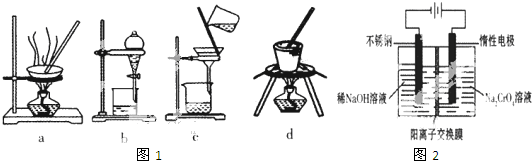
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaOH(固体) |
| B、H2O |
| C、HCl |
| D、CH3COONa(固体) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| Na、Mg、Al等物质的量 x mol | x<
|
| (3) | (4) | ||||
| H2的体积 | (1) | (2) | VNa>VMg=VAl | VNa=VMg=VAl |
查看答案和解析>>
科目:高中化学 来源: 题型:
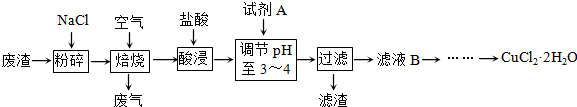
| ||
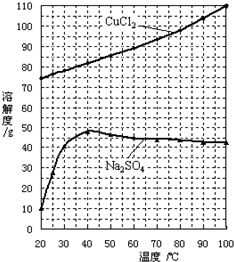
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Q2>Q1=92.4kJ |
| B、Q2=Q1=92.4kJ |
| C、Q2<Q1<92.4kJ |
| D、Q2=Q1<92.4kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com