
【题目】下列离子方程式中,正确的是( )
A.氯气通入水中,溶液呈酸性:Cl2+H2O ![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
B.用铜做电极电解CuSO4溶液:2Cu2++2H2O![]() 2Cu +O2↑+4H+
2Cu +O2↑+4H+
C.NaHS电离方程式:NaHS ![]() Na++HS-
Na++HS-
D.NH4Cl水解反应:NH4+ +2H2O ![]() NH3·H2O+H3O+
NH3·H2O+H3O+
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】金属晶体和离子晶体是重要的晶体类型。下列关于它们的说法正确的是( )
A.金属晶体和离子晶体都能导电
B.在镁晶体中,1个Mg2+只与2个自由电子存在强烈的相互作用
C.金属晶体和离子晶体都可采取密堆积方式
D.金属晶体和离子晶体中分别存在金属键和离子键等,化学键很难断裂,因而都具有延展性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数递增的短周期主族元素,Y的简单气态氢化物水溶液呈弱碱性, Z元素无正价,且基态原子有2个未成对电子,基态W原子价层电子排布式为nsn-1npn-1 ,X与W为同主族元素。基态R原子M能层全充满且核外有且仅有1个未成对电子。请回答下列问题:
(1)基态R原子的核外电子排布式为____________________。R单质晶体晶胞的堆积方式_______________,晶胞的空间利用率为___________________。
(2) X、Y、Z三种元素的第一电离能由小到大的顺序为__________ (填“元素符号”,下同)
(3)YF3分子中Y的杂化类型为______________。该分子的空间构型为_________________。
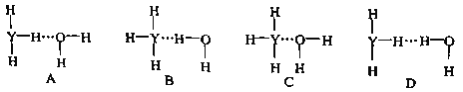
(4)Y的气态氢化物在水中可形成氢键,其氢键最可能的形式为___________________。
(5)X的某气态氧化物的相对分子质量为44,分子中的大π键可用符号Π![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则其气态氧化物中的大π键应表示为_______________,其中σ键与π数目之比为______________。
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则其气态氧化物中的大π键应表示为_______________,其中σ键与π数目之比为______________。
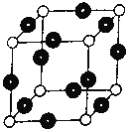
(6)R元素与Y元素形成某种化合物的晶胞结构如图所示(黑球代表R原子),若该晶体的密度为ρg·cm-3,则该晶胞的边长是_________cm (NA表示阿伏伽德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙、丙三种溶液,可能是KCl、NaBr、KI。向甲中加入淀粉溶液和氯水,溶液变为橙色,再加入丙,颜色无明显变化,则甲、乙、丙依次含有
A.NaBr、KCl、KIB.NaBr、KI、KClC.KI、NaBr、KClD.KCl、KI、NaBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是( )
A. 由乙烯分子组成和结构推测含一个碳碳双键的单烯烃通式为CnH2n
B. 乙烯的电子式为:![]()
C. 从乙烯与溴发生加成反应生成1,2—二溴乙烷可知乙烯分子的碳碳双键中有一个键不稳定,易发生断裂
D. 乙烯在空气中燃烧的现象与甲烷不同的原因是乙烯中含碳量高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下硝酸铵受热分解的化学方程式为:5NH4NO3 ![]() 2HNO3+4N2+9H2O,在反应中被氧化与被还原的氨原子数之比为( )
2HNO3+4N2+9H2O,在反应中被氧化与被还原的氨原子数之比为( )
A.5:3
B.5:4
C.1:1
D.3:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图![]() 为直流电源,
为直流电源,![]() 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸,![]() 为电镀槽,接通电路后发现
为电镀槽,接通电路后发现![]() 上的c点显红色,为实现铁上镀锌,接通
上的c点显红色,为实现铁上镀锌,接通![]() 后,使c、d两点短路,下列叙述正确的是( )
后,使c、d两点短路,下列叙述正确的是( )

A. a为直流电源的负极
B. f电极为锌板
C. c极发生的反应为2H++2e-=H2↑
D. e极发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我校化学实验室欲用NaOH固体配制1.0molL﹣1的NaOH溶液240mL:
(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容
其正确的操作顺序为 . 本实验必须用到的仪器除天平、药匙、玻璃棒、烧杯、胶头滴管等外,还需要的仪器有 .
(2)某同学欲称量NaOH固体,他先用托盘天平称量、烧杯的质量,天平平衡后的状态如图所示.烧杯的实际质量为 g,要完成本实验该同学应称取 g NaOH.
(3)使用容量瓶前必须进行的一步操作是 .
(4)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏大的是
A.转移溶液时不慎有少量洒到容量瓶外面
B.定容时俯视刻度线
C.未冷却到室温就将溶液转移到容量瓶并定容
D.定容后塞上瓶塞反复摇匀静置后,液面低于刻度线,再加水至刻度线.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com