
铜粉放入稀硫酸溶液中,加热后无明显现象发生.当加入一种盐后,铜粉的质量减少,溶液呈蓝色,同时有气体逸出.该盐是( )
|
| A. | Fe2(SO4)3 | B. | Na2CO3 | C. | KNO3 | D. | FeSO4 |
考点:
铜金属及其重要化合物的主要性质.
专题:
元素及其化合物.
分析:
Cu与稀硫酸不反应,硝酸盐在酸性条件下具有硝酸的强氧化性,则可使Cu溶解,由发生的氧化还原反应可知生成的气体,以此来解答.
解答:
解:A.Cu、稀硫酸、硫酸铁混合时,铜和硫酸铁发生氧化还原反应,生成硫酸亚铁和硫酸铜,造成铜粉的质量减少,但没有气体,故A错误;
B.Cu与稀硫酸不反应,加入Na2CO3时与酸反应生成二氧化碳气体,但Cu不溶解,故B错误;
C.Cu、稀硫酸、KNO3混合时发生3Cu+8H++2NO3﹣═3Cu2++2NO↑+4H2O,则铜粉质量减轻,同时溶液逐渐变为蓝色,且有气体逸出,故C正确;
D.Cu、稀硫酸、FeSO4混合时不反应,故D错误.
故选C.
点评:
本题考查硝酸盐在酸性条件下的性质,明确选项中各物质的性质及发生的化学反应是解答本题的关键,难度不大.


科目:高中化学 来源: 题型:
下列说法正确的是( )
A. 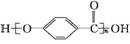 的结构中含有酯基
的结构中含有酯基
B.顺—2—丁烯和反—2—丁烯的加氢产物不同
C.1 mol葡萄糖可水解生成2 mol乳酸(C3H6O3)
D.油脂和蛋白质都是能发生水解反应的高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关叙述中正确的是( )
A.煤经过气化和液化两个物理变化,可变为清洁能源
B.葡萄糖可以制乙醇,两者都能与金属钠反应
C.明矾可用于水的消毒、杀菌;碳酸钡可用于钡餐透视
D.合成纤维和光导纤维都是有机高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组拟制备K3[Fe(C2O4)3]·3H2O晶体
Ⅰ.查 阅资料
阅资料
K3[Fe(C2O4)3]·3H2O是翠绿色晶体,易溶于水,难溶于乙醇,具有光敏性,光照分解。
110℃失去结晶水,230℃时分解。K3[Fe(C2O4)3]·3H2O的摩尔质量是491g/moL
Ⅱ.制备产品
实验步骤如下:
① 取27.8gFeSO4·7H2O和K2C2O4反应生成草酸亚铁
② 将草酸亚铁(FeC2O4)和适量K2C2O4的混合溶液置于40℃的恒温水浴中,逐滴加入 6% H2O2,边加边搅拌,使Fe2+充分被氧化。反应体系中生成K3[Fe(C2O4)3]的同时还有部分
Fe(OH)3沉淀
③ 向②所得浊液中加入1mol/LH2C2O4溶液,使溶液变为翠绿色
④ 加热浓缩,冷却结晶,过滤,洗涤,干燥,称量产品的质量为ag
请回答下列问题:
(1)第②步需要控制水浴40℃,温度不能太高的主要目的: ,若第④ 步冷却时间较长,需将溶液置于冷暗处,原因是: 。
步冷却时间较长,需将溶液置于冷暗处,原因是: 。
(2)第②步中,为检验Fe2+是否已完全被氧化,可选用 。试剂(填字母)
A. NaOH溶液 B. K3Fe(CN)6溶液 C. 苯酚溶液 D. KSCN溶液
(3)请写出第③步中加入H2C2O4溶液将Fe(OH)3沉淀反应生成K3[Fe(C2O4)3]的化学反应方程式: 。
(4)步骤④中的实验操作需要下列仪器中的 (填仪器的编号).
①酒精灯 ②燃烧匙 ③烧杯 ④广口瓶 ⑤研钵 ⑥玻璃棒
(5)有同学为提高产率,避免第④步加热浓缩过程中K3[Fe(C2O4)3]的少量分解,依 据查阅的资料提出新的结晶方案:将步骤③得到的溶液中加入 ,过滤,洗涤,干燥,称量。
据查阅的资料提出新的结晶方案:将步骤③得到的溶液中加入 ,过滤,洗涤,干燥,称量。
查看答案和解析>>
科目:高中化学 来源: 题型:
最近意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子.N4分子结构如图,已知断裂1molN﹣N吸收167kJ热量,生成1mol N≡N放出942kJ热量.根据以上信息和数据,则由N2气体生成1mol气态N4的△H为( )
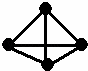
|
| A. | ﹣441kJ•mol﹣1 | B. | +441kJ•mol﹣1 | C. | ﹣882kJ•mol﹣1 | D. | +882kJ•mol﹣1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
|
| A. | 核外电子排布完全相同的两种微粒,其化学性质一定相同 |
|
| B. | 同周期的主族元素从左到右,非金属性逐渐增强,气态氢化物稳定性逐渐增强 |
|
| C. | 元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素 |
|
| D. | 原子最外层电子数大于4的元素一定是非金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,可逆反应3X(g)+Y(g)⇌2Z(g)达到限度的标志是( )
|
| A. | 单位时间内生成3nmolX,同时消耗nmolY |
|
| B. | X、Y、Z的浓度相等 |
|
| C. | X的生成速率与Z的生成速率相等 |
|
| D. | X、Y、Z的分子个数比为3:1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A. 摩尔是物质的数量单位,含有6.02×1023个微粒的物质叫做1摩尔
B. 1mol氧含有6.02×1023个氧原子
C. 在标准状况下,任何物质的摩尔体积约为22.4L/mol
D. 一定质量的气体的体积随压强增大和温度降低而变小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com