
| A. | Q 1>Q 2 | B. | Q 1=Q 2 | C. | Q 1<Q 2 | D. | 无法确定 |
分析 已知CuSO4•5H2O(s)=CuSO4(s)+5H2O(l)△H=+Q1kJ/mol;CuSO4(s)=Cu2+(aq)+SO42-(aq)△H=-Q2kJ/mol;
胆矾溶于水时,溶液温度降低,反应为CuSO4•5H2O(s)=Cu2+(aq)+SO42-(aq)+5H2O(l)△H′>0;根据盖斯定律确定△H′与Q1、Q2的关系.
解答 解:已知①CuSO4•5H2O(s)=CuSO4(s)+5H2O(l)△H=+Q1kJ/mol;
②CuSO4(s)=Cu2+(aq)+SO42-(aq)△H=-Q2kJ/mol;
③CuSO4•5H2O(s)=Cu2+(aq)+SO42-(aq)+5H2O(l)△H′>0;
根据盖斯定律:方程③=方程①+方程②,
所以△H′=Q1+(-Q2)>0,即Q1>Q2,
故选A.
点评 本题考查了物质溶解恒容物质分解过程中的能量变化,根据盖斯定律分析物质溶解过程中的能量变化是解题关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
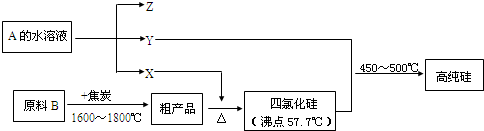
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 干冰、冰、金属钠 | B. | 二氧化硅、食盐、硫 | ||
| C. | 金刚石、碘、氧化钙 | D. | HF、HCl、HBr |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 试管1:滴加3滴浓硫酸 | 试管2:滴加3滴NaOH溶液 | |
| 实验现象 | ||
| 实验结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
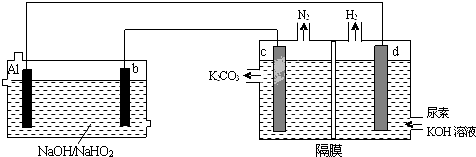
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔点1070℃,易溶于水,水溶液能导电 | |
| B. | 熔点1128℃,沸点4446℃,硬度很大 | |
| C. | 熔点10.31℃,液态不导电,水溶液能导电 | |
| D. | 熔点97.81℃,质软,导电,密度0.97g/cm3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时化学能转化为电能 | B. | 负极反应为:Li-e=Li+ | ||
| C. | 正极反应为:I2+2e-=2I- | D. | 电流由负极流向正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
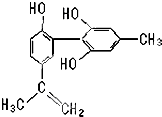 我国支持“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
我国支持“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )| A. | 遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 | |
| B. | 该分子中的所有碳原子不可能共平面 | |
| C. | 滴入KMnO4(H+)溶液,观察紫红色变浅,仅是因为结构中存在碳碳双键 | |
| D. | 1mol该物质分别与浓溴水和H2反应时最多消耗Br2和 H2分别为4mol、7mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com