
【题目】阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是( )
A. 2.24LCO2中含有的原子数为0.3 ×6.02×1023
B. 0.1L3 mol·L-1的NH4NO3溶液中含有的NH4+数目为0.3 ×6.02×1023
C. 5.6g铁粉与硝酸反应失去的电子数一定为0.3 ×6.02×1023
D. 4.5 SiO2晶体中含有的硅氧键数目为0.3 ×6.02×1023
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】第四届中国工业大奖于2016年12月11日在北京颁奖,获奖项目之一为国家级一类抗癌新药——盐酸埃克替尼的研发。它的关键中间体G的一种合成路线如下:

己知:①A分子中只有一种化学环境的氢;
②TsCl为![]() 。
。
(1)A的名称为______________。
(2)G中所含官能团的名称是______________; E的结构简式为___________________。
(3)由B生成C的反应类型是_____________,由F生成G的反应类型是______________。
(4)PEO是由A在烃基铝催化下加聚而成的线型髙分子,该加聚反应的化学方程式为_______________。
(5)三取代芳香族化合物W是D的同分异构体。W既能发生银镜反应和水解反应,又能与FeCl3溶液发生显色反应。1molW最多可与4molNaOH反应,W的核磁共振氢谱只有4组峰。W的结构简式为_________________。
(6)参照上述合成路线, 以邻硝基甲苯( )和乙醇为原料(无机试剂任选),设计制备邻氨基苯甲酸乙酯(
)和乙醇为原料(无机试剂任选),设计制备邻氨基苯甲酸乙酯(![]() )的合成路线。_________________
)的合成路线。_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 加热TiCl4浓溶液制备TiO2·xH2O:Ti4++(x+2)H2O![]() TiO2·xH2O+4H+
TiO2·xH2O+4H+
B. (NH4)2Fe(SO4)2溶液中加入少量KOH溶液:![]()
C. 钢铁发生吸氧腐蚀时的正极反应:O2+4H++4e-=2H2O
D. 酸性KI溶液中通入O2:4H++2I-+O2=2H2O+I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.控制变量法是化学实验中的—种常用方法,如表是某课外兴趣小组研究等物质的量浓度的稀硫酸和锌反应的实验数据(计算结果精确到小数点—位),分析以下数据,回答下列问题:
序号 | 硫酸的体积 /mL | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于酸的 时间/s | 生成硫酸锌的质量/g |
① | 50.0 | 2.0 | 薄片 | 15 | 200 | m1 |
② | 50.0 | 2.0 | 薄片 | 25 | 100 | m2 |
③ | 50.0 | 2.0 | 颗粒 | 25 | 70 | m3 |
④ | 50.0 | 2.0 | 颗粒 | 35 | 35 | m4 |
⑤ | 50.0 | 2.0 | 粉末 | 25 | t1 | 5.0 |
⑥ | 50.0 | 4.0 | 粉末 | 25 | t2 | m5 |
⑦ | 50.0 | 6.0 | 粉末 | 25 | t3 | 14.9 |
⑧ | 50.0 | 8.0 | 粉末 | 25 | t4 | 19.3 |
⑨ | 50.0 | 10.0 | 粉末 | 25 | t5 | 19.3 |
(1)实验①和实验②表明_____对反应速率有影响;研究锌的形状对反应速率的影响时,最好选取实验_______ (填3个实验序号)。
(2)下列数据推断正确的是______________________。
A. t1<70 B.t1>t4 C.m12 D.m6=19.3
(3)若采用与实验①完全相同的条件,但向反应窗口中滴加少量硫酸铜溶液,发现反应速率明显加快,原因是___________________________________。
(4)根据表中数据计算:硫酸的物质的量浓度是_________________mol/L。
II.己知在 25℃、l0l kPa 下,2NO(g)+2CO(g) ![]() N2(g)+2CO2(g),现将 2molNO、2.4molCO通入恒容密闭容器中,反应过程中部分物质的浓度变化如图所示。
N2(g)+2CO2(g),现将 2molNO、2.4molCO通入恒容密闭容器中,反应过程中部分物质的浓度变化如图所示。
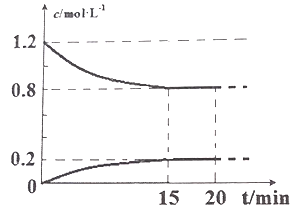
(1) 015min 内,v(CO2) =__________________。
(2)该反应的速率时间图像如下图中左图所示。若其他条件不变,仅在反应前加入合适的催化剂,其速率时间图像如下图中右图所示。以下说法正确的是______(填对应字母)。
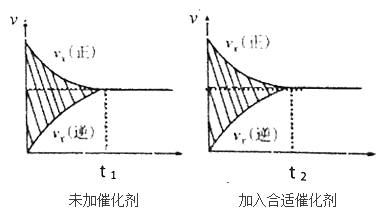
A.a1>a2 B.b12 C.t1>t2
(3) 一定条件下,己知反应NO2(g)+SO2(g) ![]() NO(g)+SO3(g),将NO2
NO(g)+SO3(g),将NO2
a.体系压强保持不变 b.混合气体颜色保持不变
c.NO2与SO2的体积比保持不变 d.每消耗lmol SO2的同时生成lmol NO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com