
| A.IA族 | B.ⅡA族 | C.ⅢA族 | D.IVA族 |
科目:高中化学 来源:不详 题型:填空题
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 原子最外层电子数是次外层的三倍 |
| Z | 单质及其化合物的焰色反应为黄色 |
| W | W元素基态原子的M层全充满,N层只有一个电子 |
 。X的一种单质熔点很高,硬度很大,则这种单质的晶体属于 晶体。
。X的一种单质熔点很高,硬度很大,则这种单质的晶体属于 晶体。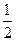 O2(g) ="=" H2O(l) ΔH= -285.8kJ·mol-1
O2(g) ="=" H2O(l) ΔH= -285.8kJ·mol-1查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.n="m+1" | B.n=m+11 | C.n="m+25" | D.n=m+10 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子半径:Na+>Mg2+>Al3+ | B.还原性:Cl->Br->I- |
| C.酸性:HClO4>H2SO4>H3PO4 | D.碱性:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素的非金属性:S>Cl>P>Si |
| B.元素第一电离能:O<N<F |
| C.离子半径:Al3+>Mg2+>Na+ |
| D.沸点:HCl<HBr<HF |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.还原性: X的氧化物﹥Y的氧化物﹥Z的氢化物 |
| B.简单离子的半径:M的离子﹥Z的离子﹥Y的离子﹥X的离子 |
| C.Y X2﹑ M2Y都是含有极性键的极性分子 |
| D.Z元素的最高价氧化物的水化物的化学式为HZO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 A质子数、B中子数、C质子数和中子数、D最外层电子数、E电子层数,请用单个序号填写下列各空白。
A质子数、B中子数、C质子数和中子数、D最外层电子数、E电子层数,请用单个序号填写下列各空白。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com