
100mL 6mol/L H2SO4跟过量锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的()
A. 碳酸钠(固体) B. 石灰水 C. 硫酸钾溶液 D. 硫酸铵(固体)
考点: 化学反应速率的影响因素.
专题: 化学反应速率专题.
分析: 根据反应的实质为Zn+2H+═Zn2++H2↑,为了减缓反应速率,但又不影响生成氢气的总量,则减小氢离子的浓度但不能改变氢离子的物质的量即可,注意Zn过量,以此来解答.
解答: 解:A.碳酸钠与酸反应,生成氢气的量减少,故A错误;
B.石灰水与酸反应,生成氢气的量减少,故B错误;
C.加适量的K2SO4溶液,相当于稀释,氢离子的物质的量不变,浓度变小,则减缓反应进行的速率,但又不影响生成氢气的总量,故C正确;
D.加硫酸铵,Zn与铵根离子水解生成的氢离子反应生成氢气,反应速率加快,氢气的量增大,故D错误.
故选C.
点评: 本题考查影响化学反应速率的因素,明确浓度对反应速率的影响即可解答,选项D为学生解答中的难点,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年浙江省高三4月阶段测试理综试卷化学试卷(解析版) 题型:选择题
某溶液X中可能含有NO3-、Cl-、SO42-、CO32-、NH4+、Fe2+、Fe3+、Al3+和K+中的几种,且所含阴离子的物质的量相等。为确定该溶液X的成分,某学习小组做了如下实验:
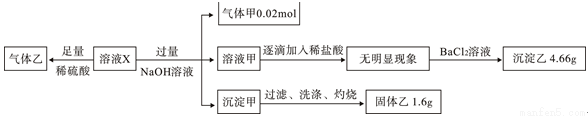
则下列说法正确的是
A.若含有Fe3+,则一定含有Cl-
B.SO42-、NH4+一定存在,NO3-、Cl–可能不存在
C.CO32-、Al3+、K+一定不存在
D.气体甲、沉淀甲一定为纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应aA(s)+bB(g)⇋cC(g)+dD(g)△H=Q kJ•mol﹣1,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示,据图分析,以下正确的是( )
|
| A. | T1>T2,Q>0 | B. | T1<T2,Q<0 |
|
| C. | p1>p2,a+b=c+d | D. | p1<p2,a+b=c+d |
查看答案和解析>>
科目:高中化学 来源: 题型:
关于活化分子说法错误的是()
A. 发生有效碰撞的分子一定是活化分子
B. 活化分子间的碰撞一定是有效碰撞
C. 能发生有效碰撞的分子必须具有相当高的能量
D. 使用催化剂能改变分子的活化能
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学反应速率的说法,不正确的是()
A. 化学反应速率是衡量化学反应进行快慢程度的物理量
B. 化学反应速率的大小主要取决于反应物的性质
C. 化学反应速率常用单位时间内生成某物质的质量的多少来表示
D. 化学反应速率常用单位有:mol•L﹣1•s﹣1和mol•L﹣1•min﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组要完成中和热的测定.
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5mol•L﹣1
盐酸、0.55mol•L﹣1NaOH溶液,实验尚缺少的玻璃用品是.
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?(填“能”或“否”),其原因是
(3)他们记录的实验数据如下:
实验用品 溶液温度 中和热
t1 t2 △H
① 50 mL
0.55 mol•L﹣1
NaOH溶液 50 mL
0.5 mol•L﹣1
HCl溶液 20℃ 23.3℃
﹣56.8kJ/mol
② 50 mL
0.55 mol•L﹣1
NaOH溶液 50 mL
0.5 mol•L﹣1
HCl溶液 20℃ 23.5℃
已知:Q=c m(t2﹣t1),反应后溶液的比热容c为4.18kJ•℃﹣1•kg﹣1,各物质的密度均为1g•cm﹣3.
①计算完成上表.
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:.
(4)若用KOH代替NaOH,对测定结果无(填“有”或“无”)影响;若用醋酸代替HCl做实验,对测 定结果(填“有”或“无”)影响.
(5)已知H+(aq)+OH﹣(aq)═H2O(l)△H=﹣57.3kJ/mol,回答下列问题.
①用含20g NaOH的稀溶液跟足量稀盐酸反应放出kJ的热量.
②用含2mol H2SO4的稀溶液跟足量稀NaOH反应,此反应的中和热△H为.
③如果将反应中的稀盐酸换成稀醋酸,反应放出的热量(填“大于”、“小于”或“等于”)放出的热量.
查看答案和解析>>
科目:高中化学 来源: 题型:
现有A、B、C、D、E、F、G、H、M九种物质,其中A、B、C均为氧化物,且A为淡黄色粉末,G、E为气体单质,F的水溶液与石灰水混合可制得D的溶液。它们之间相互转化关系如图所示,其他与题目无关的生成物均已略去。
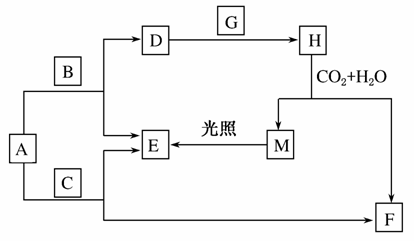
请回答下列问题:
(1)写出化学式:H________,C________。
(2)写出下列反应的化学方程式:
A+C→F+E________________________________________;
F+Ca(OH)2→D_____________________________________。
(3)写出离子反应方程式:D+G→H____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com