
 ;二氧化碳中存在两对碳氧共用电子对,二氧化碳的电子式为:
;二氧化碳中存在两对碳氧共用电子对,二氧化碳的电子式为: ,
, ;
; ;
; ;氮气是氮原子间形成氮氮三键,氮气的结构式为N≡N,
;氮气是氮原子间形成氮氮三键,氮气的结构式为N≡N, ;N≡N;
;N≡N;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
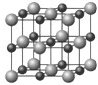 CrO2Cl2在有机合成中可作氧化剂或氯化剂,能与许多有机物反应,可用重铬酸钾与四氯化碳反应制备:
CrO2Cl2在有机合成中可作氧化剂或氯化剂,能与许多有机物反应,可用重铬酸钾与四氯化碳反应制备:查看答案和解析>>
科目:高中化学 来源: 题型:
| 酸 | 电离方程式 | 电离平衡常数K |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.76×10-5 |
| HClO | HClO?ClO-+H+ | 2.95×10-8 |
| H2S | H2S?H++HS- HS-?H++S2- | K1=9.1×10-8 K2=1.1×10-12 |
| H2CO3 | H2CO3?H++HCO3- HCO3-?H++CO32- | K1=4.31×10-7 K2=5.61×10-11 |
| H3PO4 | H3PO4?H++H2PO4- H2PO4-?H++HPO42- HPO42-?H++PO43- | K1=7.1×10-3 K2=6.3×10-8 K3=4.2×10-13 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、M>N>P |
| B、P>N>M |
| C、P>M>N |
| D、N>M>P |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com